
【题目】下列离子方程式正确的是( )
A.鸡蛋壳溶于食醋:CaCO3+2CH3COOH→(CH3COO)2Ca+H2O+CO2↑
B.苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O﹣→2C6H5OH+CO32﹣
C.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH﹣ ![]() CH2BrCOO﹣+H2O
CH2BrCOO﹣+H2O
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH﹣ ![]() CH3COO﹣+NH4++3NH3+2Ag↓+H2O
CH3COO﹣+NH4++3NH3+2Ag↓+H2O
【答案】D
【解析】解:A.碳酸钙和醋酸都需要保留化学式,醋酸钙应该拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO﹣ , 故A错误;
B.苯酚钠溶液中通入少量CO2 , 反应生成苯酚和碳酸氢钠,正确的离子方程式为:CO2+H2O+C6H5O﹣→C6H5OH+HCO3﹣ , 故B错误;
C.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热,Br原子也参与反应,正确的离子方程式为:CH2BrCOOH+2OH﹣ ![]() CH2(OH)COO﹣+H2O+Br﹣ , 故C错误;
CH2(OH)COO﹣+H2O+Br﹣ , 故C错误;
D.用银氨溶液检验乙醛中的醛基,反应的离子方程式为:CH3CHO+2Ag(NH3)2++2OH﹣ ![]() CH3COO﹣+NH4++3NH3+2Ag↓+H2O,故D正确;
CH3COO﹣+NH4++3NH3+2Ag↓+H2O,故D正确;
故选D.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】将4g NaOH溶解在10mL水中,再稀释成1L,从中取1mL,这1mL溶液的物质的量浓度为( )
A.1molL﹣1
B.0.1molL﹣1
C.0.01molL﹣1
D.10molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯发生的下列反应中,不属于加成反应的是 ( )
A. 与氢气反应生成乙烷
B. 与水反应生成乙醇
C. 与溴水反应使之褪色
D. 与氧气反应生成二氧化碳和水
查看答案和解析>>
科目:高中化学 来源: 题型:
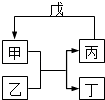
【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )
甲 | 乙 | 丙 | 戊 | |
① | NH3 | O2 | NO | H2O |
② | Fe | H2O | H2 | Fe2O3 |
③ | Al2O3 | NaOH溶液 | NaAlO2溶液 | 过量CO2 |
④ | Na2O2 | CO2 | O2 | Na |
A.①③
B.②③
C.②④
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NiSO46H2O是一种绿色易溶于水的晶体,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得.操作步骤如下:
(1)向滤液Ⅰ中加入FeS是为了生成难溶于酸的硫化物沉淀而除去Cu2+、Zn2+等杂质,则除去Cu2+的离子方程式为: .
(2)对滤液Ⅱ的操作,请回答:
①往滤液Ⅱ中加入H2O2的离子方程式: .
②调滤液ⅡpH的目的是除去Fe3+ , 其原理是Fe3++3H2OFe(OH)3+3H+ , 已知25℃时Ksp[Fe(OH)3]=2.8×10﹣39 , 则该温度下上述反应的平衡常数K=
③检验Fe3+是否除尽的操作和现象是 .
(3)滤液Ⅲ溶质的主要成分是NiSO4 , 加Na2CO3过滤后得到NiCO3固体,再加适量稀硫酸溶解又生成NiSO4 , 这两步操作的目的是 .
(4)得到的NiSO4溶液经一系列操作可得到NiSO46H2O晶体,请回答:
①一系列操作主要包括、、等操作.
②为了提高产率,过滤后得到的母液要循环使用,则应该回流到流程中的位置.(填a、b、c、d)
③如果得到产品的纯度不够,则应该进行操作(填操作名称).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由C16O和C18O组成的混合气体与同温、同压下空气(平均相对分子质量为29)的密度相同,则下列关系正确的是( )
A.混合气体中C16O和C18O的分子数之比为14:15
B.混合气体中C16O和C18O的物质的量之比为1:1
C.混合气体中C16O和C18O的质量之比为15:14
D.混合气体中C16O和C18O的密度之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使石蕊试液变红的溶液中:I﹣、MnO4﹣、NO3﹣、Na+
B.含有大量Fe3+的溶液:NH4+、HCO3﹣、SO42﹣、AlO2﹣
C.水电离出C(H+)=1.0×10﹣12mol/L 的溶液:Cl﹣、Na+、ClO﹣、NH4+
D.澄清透明的溶液:Cu2+、Fe3+、SO42﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答:
(1)氢氧燃料电池的能量转化主要形式是 , 在导线中电子流动方向为(用a、b表示).
(2)负极反应式为 .
(3)电极表面镀铂粉的原因为 .
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一.金属锂是一种重要的储氢材料,吸氢和放氢原理如下: I.2Li+H2 ![]() 2LiH
2LiH
Ⅱ.LiH+H2O═LiOH+H2↑
①反应I中的还原剂是 . 反应Ⅱ中的氧化剂是 .
②已知LiH固体密度为0.82g/cm3 . 用镁吸收224L(标准状况)H2 , 生成的LiH体积与被吸收的H2体积比为 .
③由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com