
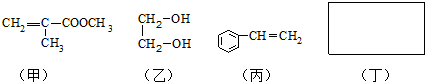
| 稀硫酸 |
| △ |
| 一定条件 |
| 浓硫酸 |
| 170℃ |
| 试剂X |
| NaOH溶液 |
| △ |
 );含C=C能发生加成和氧化反应,与AC中物质反应褪色,甲的同分异构体中一种不含甲基的羧酸,含C=C和-COOH,其结构简式为CH2=CH-CH2-CH2-COOH,
);含C=C能发生加成和氧化反应,与AC中物质反应褪色,甲的同分异构体中一种不含甲基的羧酸,含C=C和-COOH,其结构简式为CH2=CH-CH2-CH2-COOH, );AC;CH2=CH-CH2-CH2-COOH;
);AC;CH2=CH-CH2-CH2-COOH; ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生铁比纯铁更易生锈 |
| B、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| C、银质奖章久置后易表面变暗 |
| D、海轮上一般会在吃水线下绑定一定量的锌块 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y的基态原子最外层电子排布式为nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com