
【题目】![]() 是常规核裂变产物之一,可以通过测定大气或水中的含量变化来监测核电站是否发生放射性物质泄漏.下列有关有叙述中错误的是( )
是常规核裂变产物之一,可以通过测定大气或水中的含量变化来监测核电站是否发生放射性物质泄漏.下列有关有叙述中错误的是( )
A.![]() 的化学性质与
的化学性质与 ![]() 是相同
是相同
B.![]() 的原子序数为53
的原子序数为53
C.![]() 的原子核外电子数为78
的原子核外电子数为78
D.![]() 的原子核内中子数多于质子数
的原子核内中子数多于质子数
【答案】C
【解析】解:A. ![]() 与
与 ![]() 质子数相同,中子数不同,互为同位素,化学性质几乎完全相同,物理性质有差别,故A正确;
质子数相同,中子数不同,互为同位素,化学性质几乎完全相同,物理性质有差别,故A正确;
B.原子符号AZX左下角数字代表质子数, ![]() 的质子数为53,原子序数为53,故B正确;
的质子数为53,原子序数为53,故B正确;
C. ![]() 是电中性原子,质子数等于原子核外电子数为53,故C错误;
是电中性原子,质子数等于原子核外电子数为53,故C错误;
D. ![]() 的质子数为53,中子数=131﹣53=78,中子数多于质子数,故D正确.
的质子数为53,中子数=131﹣53=78,中子数多于质子数,故D正确.
故选C.
A.互为同位素的原子化学性质几乎完全相同,物理性质有差别;
B.原子符号AZX左下角数字代表质子数,左上角数字代表质量数,X代表元素符号;
C.电中性原子质子数等于核外电子数;
D.原子符号AZX左下角数字代表质子数,左上角数字代表质量数,X代表元素符合.根据质量数=质子数+中子数计算中子数.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】A,B,C,D四种短周期元素,原子序数D>A>B>C,且A,B同周期,C,D同主族,A的原子结构示意图为: 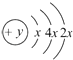 ,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
(1)A的元素名称为 , 其气态氢化物的稳定性比CH4(填“强”或“弱”).
(2)C,D的最高价氧化物的水化物的酸性大小为>(填化学式).
(3)B的活泼性比钙的(填“强”或“弱”).
(4)写出C的气态氢化物与其最高价氧化物对应的水化物反应 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中化学键的类型相同的是( )
A. HCl、MgCl2、NH4Cl B. NH3、H2O、CO2
C. H2O、Na2O、CO2 D. CaCl2、NaOH、H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组以难溶性钾长石(K2O·Al2O3·6SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下:

(1)煅烧过程中有如下反应发生:
①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式: _______ 。
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式:________________________________。
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2-+ 2H2O![]() Al(OH)3+OH-。“浸取”时应保持溶液呈____性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_______________________________________。
Al(OH)3+OH-。“浸取”时应保持溶液呈____性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_______________________________________。
(3)“转化”时加入NaOH的主要作用是(用离子方程式表示)___________________。
(4)上述工艺中可以循环利用的主要物质是 _________ 、___________和水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个体积均为1.0L的恒容密闭容器中反应:2H2(g)+CO(g) ![]() CH3OH(g)达到平衡。下列说法正确的是( )
CH3OH(g)达到平衡。下列说法正确的是( )
容器 | 温度/K | 物质的起始浓度/molL–1 | 物质的平衡浓度/molL-1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
I | 500 | 0.40 | 0.20 | 0 | 0.160 |
II | 500 | 0.80 | 0.40 | 0 | |
III | 800 | 0 | 0 | 0.20 | 0.050 |
A. 该反应的正反应为吸热反应
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大
C. 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com