
【题目】化学与人类的生活息息相关,下列有关说法正确的是
A.因铝表面能形成致密的氧化膜,所以铝制餐具可以长期使用
B.有机玻璃(聚甲基丙烯酸甲酯)是通过缩聚反应制得的
C.SiO2用途广泛,因其高熔点的特性成为光导纤维的主要原料
D.因废弃物易污染环境,腈纶不宜大量取代棉、麻等天然材料
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】现有下列短周期元素性质的数据:
元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
最高或 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
-2 | -3 | -1 | -3 |
下列说法正确的是
A.原子序数⑦元素大于④元素
B.②、③处于同一周期
C.上述八种元素最高价氧化物对应的水化物,⑤号酸性最强
D.⑧号元素原子结构示意图为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素的性质及其递变规律正确的是( )
A. 同主族元素形成的单质熔沸点自上而下逐渐升高
B. 核外电子排布相同的微粒化学性质不一定相同
C. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
D. 非金属元素的气态氢化物的稳定性越强其沸点就越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合利用CO2、CO对构建低碳社会有重要意义。
(1)利用H2 和CO在一定条件下发生如下反应:CO(g) +2H2(g)![]() CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
①10min后达到平衡时CO的浓度为 ;
②10min内用H2表示的平均反应速率为 ;
(2)利用H2 和CO2在一定条件下可以合成乙烯:
6H2+2CO2![]() CH2=CH2+4H2O为放热反应
CH2=CH2+4H2O为放热反应
① 不同温度对CO2的转化率及催化剂的催化效率的影响如图所示。

下列有关说法不正确的是 (填序号)。
A.不同条件下反应,N点的速率最大
B.温度在约250℃时,催化剂的催化效率最高
C.相同条件下,乙烯的产量M点比N高
②若在密闭容器中充入体积比为 3∶1的 H2和CO2,则图中M点时,产物
CH2=CH2的体积分数为 。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 乙烷和乙烯均可使酸性KMnO4溶液褪色
B. 纤维素、淀粉和蛋白质都是高分子化合物
C. 煤的干馏和石油的分馏均属化学变化
D. 酯类和糖类均能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的 石油化工水平。请回答下列问题。
(1)乙烯的结构简式____________。
(2)鉴别甲烷和乙烯的试剂是______(填序号)。
A.稀硫酸
B.溴的四氯化碳溶液
C.水
D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是______(填序号)。
A.CH3CH3 B.CH3CHCl2 C.CH3CH2OH D.CH3CH2Br
(4)已知2CH3CHO+O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其 合成路线如下图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其 合成路线如下图所示。
![]()
反应②的化学方程式为____________________________________。工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为____________________________________,反应类型是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Fe粉是新型材料,具有超强磁性、高效催化性。某化学小组探究用氢气和碳酸亚铁制取纳米级铁粉。其实验设计如图(加热、支持装置省略)
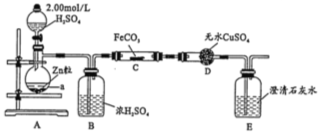
(1)a的名称是________________;浓硫酸的作用是________________。
(2)打开分液漏斗活塞,一段时间后再对C装置加热,这样操作的目的是_______________;反应一段时间后D中变蓝,E中溶液变浑浊,C中发生反应的化学方程式为______________。
(3)反应中若观察到B装置中气泡产生过快,则应进行的操作是_____________________。
(4)反应一段时间后,B中产生气泡太慢,再滴加硫酸反应速率略有加快但不明显;若向硫酸中加少量硫酸铜再滴入与Zn反应,反应速率明显加快,原因是____________________。
(5)检验碳酸亚铁中含有铁元素的实验方法是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】山梨酸(CH3-CH=CH-CH=CH-COOH)是一种常用的食品防腐剂。下列关于山梨酸性质的叙述中,不正确的是
A.可与钠反应
B.可与碳酸钠溶液反应
C.可与溴的四氯化碳溶液发生取代反应
D.可生成高分子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com