
| A、碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 |
B、由于乳酸(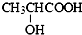 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子 |
| C、HF的稳定性很强,是因为其分子间能形成氢键 |
D、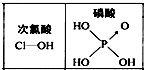 由图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子 |
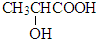 中第二个C为手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子,故B正确;
中第二个C为手性碳原子,导致该物质存在互为镜像的两个手性异构体;生产中可利用“手性合成”法主要得到其中一种手性分子,故B正确;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2是生产光导纤维和粗硅的主要原料 |
| B、工艺师利用盐酸刻蚀石英制作艺术品 |
| C、SiO2与CO2都属于酸性氧化物,都不能与酸反应 |
| D、水晶的主要成分是SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、等于196.64kJ?mol-1 |
| B、等于196.64 kJ |
| C、小于196.64kJ |
| D、大于196.64kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状态下22.4LSO3分子数为NA |
| B、常温常压下,16gO2和16gO3中所含原子数均为NA |
| C、7.8 g Na2O2含有的阴离子数是0.2NA |
| D、1L2mol?L-1的Al(NO3)3溶液中含Al3+个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温常压下,11.2LN2含有分子数为0.5NA |
| B、在常温常压下,22.4LNe含有原子数为NA |
| C、71gCl2所含有的原子数为2NA |
| D、在同温同压下,相同体积的气体单质含有原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、32gO3所含有的原子数目与1molO2所含原子物质的量相等 |
| B、4g金属钙变成钙离子时失去的电子数目为0.1NA |
| C、1molCH3+所含的电子数为10NA |
| D、标准状况下,22.4L H2O所含的分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com