
【题目】某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验:
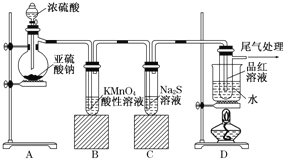
(1)装置A中盛放亚硫酸钠的仪器名称是_________,其中发生反应的化学方程式为_______。
(2)实验过程中,装置B、C中发生的现象分别是______、______,装置B中发生反应的离子方程式为_____。
(3)设计装置D的目的是________。
(4)最后用某溶液进行尾气处理,反应的离子方程式为_________________
【答案】蒸馏烧瓶 Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O 溶液由紫红色变为无色 无色溶液中出现黄色浑浊 5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+ 探究SO2与品红作用的可逆性 SO2+2OH-=SO32-+H2O
【解析】
(1)根据仪器名称书写;亚硫酸钠和浓硫酸反应生成硫酸钠、二氧化硫和水;
(2)二氧化硫能被酸性高锰酸钾氧化,能和硫化氢发生氧化还原反应生成硫单质;根据元素化合价变化判断氧化性、还原性;
(3)因二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色,装置D的目的是探究SO2与品红作用的可逆性;
(4)利用氢氧化钠溶液来吸收尾气。
(1)该仪器是蒸馏烧瓶,硫酸的酸性大于亚硫酸,根据强酸制取弱酸知,硫酸和亚硫酸钠反应生成硫酸钠、二氧化硫和水,反应方程式为:Na2SO3+H2SO4(浓)═Na2SO4+SO2↑+H2O,故答案为:蒸馏烧瓶;Na2SO3+H2SO4(浓)═Na2SO4+SO2↑+H2O。
(2)酸性高锰酸钾具有强氧化性,通入二氧化硫后溶液褪色,说明高锰酸钾将二氧化硫氧化,自身被还原,所以二氧化硫具有还原性,看到的现象是溶液由紫色变为无色,反应的离子方程式为:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+,硫化氢和二氧化硫反应生成硫单质,硫不易溶于水,所以看到无色溶液中出现淡黄色沉淀,故答案为:溶液由紫红色变为无色;无色溶液出现淡黄色浑浊;5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+。
(3)因二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色,装置D的目的是探究SO2与品红作用的可逆性,故答案为:探究SO2与品红作用的可逆性。
(4)利用氢氧化钠溶液来吸收尾气,发生的离子反应为:SO2+2OH-=SO32-+H2O,故答案为:SO2+2OH-=SO32-+H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】纯净的氮化镁(Mg3N2)是淡黄色固体,热稳定性较好,遇水极易发生反应。某同学初步设计了如下实验装置制备氮化镁(夹持及加热仪器没有画出)。
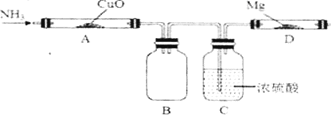
己知:Mg + 2NH3→Mg(NH2)2+H2。请回答:
(1)A中观察到的实验现象是_____________,装置C的作用除了干燥以外还有________________;
(2)下列说法不正确的是 __________
A.为了得到纯净的氮化镁,实验前需要排除装置中的空气
B.装B起到了缓冲安全的作用
C.将装罝B、C简化成装有碱石灰的U型管,也能达到实验目的
D.实验后,取D中固体加少量水,能生成使湿润的蓝色石蕊试纸变红的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列短周期元素的数据(已知Be的原子半径为0.089nm):
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
最低负化合价 | -2 | -3 | -1 | -3 |
(1)⑧号元素在周期表中的位置是______________________________;上述元素处于同一主族的有_______________________________。(用元素号表示)
(2)元素①和⑥能形成两种化合物,其中较稳定的化合物与水反应的离子方程式:_______。
(3)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等);![]() 和
和![]() 作核反应堆最佳热载体,
作核反应堆最佳热载体,![]() H和
H和![]() D用作高温堆减速剂。下列说法中正确的是___________。
D用作高温堆减速剂。下列说法中正确的是___________。
A.![]() 和
和![]() 属于同种核素
属于同种核素
B.![]() H和
H和![]() D的化学性质不同
D的化学性质不同
C.![]() H和
H和![]() D是同种物质
D是同种物质
D.氧化性:Li+<Na+<K+<Rb+<Cs+
E.碱性:Be(OH)2<LiOH<NaOH<KOH
F.半径:K>Na>Li>Li+
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:将⑦的最简单的气态氢化物通入到等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程中的总离子方程式______________。反应生成的两种碱继续作用即得到产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. NaCl ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
B. Cu ![]() CuS
CuS ![]() CuCl2
CuCl2
C. Fe2O3 ![]() FeCl3(aq)
FeCl3(aq)![]() 无水FeCl3
无水FeCl3
D. MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的铁、铝合金与300mL 2mol/L硝酸完全反应生成3.36LNO(标况)和三价铁盐、铝盐等,再向反应后的溶液中加入3mol/L的NaOH溶液,使铝、铁元素完全沉淀下来,则所加NaOH溶液的体积是( )
A. 450mL B. 150mL C. 200mL D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关试剂的保存方法,错误的是( )
A.浓硝酸保存在无色玻璃试剂瓶中
B.少量钠保存在煤油中
C.氢氧化钠溶液保存在带有橡皮塞的玻璃试剂瓶中
D.新制氯水通常保存在棕色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为 r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法中正确的是

A. X元素位于第ⅣA族
B. A能溶解于B中
C. A和C不可能发生氧化还原反应
D. B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)若A常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是________;
②在工业生产中B气体的大量排放被雨水吸收后形成______而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体.
①A、C的化学式分别是:A________;C________。
② C→D反应的化学方程式 __________________________________;该反应________(填“属于”或“不属于”)氧化还原反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com