
【题目】某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
![]()
回答下列问题:
(1)装置A中a的作用是______________;装置C中的试剂为________________;装置A中制备Cl2的化学方程为______________。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是________________。
(3)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入___________(填“酸式”或“碱式”)滴定管中;在规格为50.00mL的滴定管中,若KMnO4溶液起始读数为15.00mL,此时滴定管中KMnO4溶液的实际体积为______________(填标号)。
A.15.00 mL B.35.00mL C.大于35.00mL D.小于15.00m1
(4)某FeC2O4﹒2H2O样品中可能含有的杂质为Fe2(C2O4)3、H2C2O4﹒2H2O,采用KMnO4滴定法测定该样品的组成,实验步骤如下:
Ⅰ.取mg样品于锥形瓶中,加入稀H2SO4溶解,水浴加热至75℃。用 c mol﹒L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H2SO4酸化后,在75℃继续用KMnO4溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO4溶液V2mL。
样品中所含![]() 的质量分数表达式为_________________。
的质量分数表达式为_________________。
下列关于样品组成分析的说法,正确的是__________(填标号)。
A.![]() 时,样品中一定不含杂质
时,样品中一定不含杂质
B.![]() 越大,样品中
越大,样品中![]() 含量一定越高
含量一定越高
C.若步骤I中滴入KMnO4溶液不足,则测得样品中Fe元素含量偏低
D.若所用KMnO4溶液实际浓度偏低,则测得样品中Fe元素含量偏高
【答案】平衡气压,使浓盐酸顺利滴下; NaOH溶液 ![]() 在装置A、B之间加装盛有饱和食盐水的洗气瓶 酸式 C
在装置A、B之间加装盛有饱和食盐水的洗气瓶 酸式 C ![]() BD
BD
【解析】
漂白粉的有效成分Ca(ClO)2具有强氧化性,和浓盐酸在A中发生归中反应产生Cl2,Cl2和K2MnO4在B中反应产生KMnO4,反应不完的Cl2用C吸收,据此解答。
(1)装置A为恒压分液漏斗,它的作用是平衡气压,使浓盐酸顺利滴下,C的作用是吸收反应不完的Cl2,可用NaOH溶液吸收,Ca(ClO)2和浓盐酸在A中发生归中反应产生Cl2,反应的化学方程式为Ca(ClO)2+4HCl=CaCl2+2Cl2↑+2H2O,故答案为:平衡气压,使浓盐酸顺利滴下;NaOH溶液;Ca(ClO)2+4HCl=CaCl2+2Cl2↑+2H2O;
(2)锰酸钾在浓强碱溶液中可稳定存在,碱性减弱时易发生3MnO42-+2H2O=2MnO4-+MnO2↓+4OH-,一部分MnO42-转化为了MnO2,导致最终KMnO4的产率低,而浓盐酸易挥发,直接导致B中NaOH溶液的浓度减小,故改进措施是在装置A、B之间加装盛有饱和食盐水的洗气瓶吸收挥发出来的HCl,故答案为:在装置A、B之间加装盛有饱和食盐水的洗气瓶;
(3)高锰酸钾有强氧化性,强氧化性溶液加入酸式滴定管,滴定管的“0”刻度在上,规格为50.00mL的滴定管中实际的体积大于(50.00-15.00)mL,即大于35.00mL,故答案为:酸式;C;
(4)设FeC2O4·2H2O的物质的量为xmol,Fe2(C2O4)3的物质的量为ymol,H2C2O4·2H2O的物质的量为zmol,步骤I中草酸根和Fe2+均被氧化,结合得失电子守恒有:2KMnO4~5H2C2O4(C2O42-),KMnO4~5Fe2+,所以![]() ,步骤II中Fe2+被氧化,由KMnO4~5Fe2+可知,
,步骤II中Fe2+被氧化,由KMnO4~5Fe2+可知,![]() ,联立二个方程解得:z=2.5(cV1-3V2)×10-3,所以H2C2O4·2H2O的质量分数=
,联立二个方程解得:z=2.5(cV1-3V2)×10-3,所以H2C2O4·2H2O的质量分数=![]() =
=![]() 。关于样品组成分析如下:
。关于样品组成分析如下:
A.![]() 时,H2C2O4·2H2O的质量分数=
时,H2C2O4·2H2O的质量分数=![]() =0,样品中不含H2C2O4·2H2O,由
=0,样品中不含H2C2O4·2H2O,由![]() 和
和![]() 可知,y≠0,样品中含Fe2(C2O4)3杂质,A错误;
可知,y≠0,样品中含Fe2(C2O4)3杂质,A错误;
B.![]() 越大,由H2C2O4·2H2O的质量分数表达式可知,其含量一定越大,B正确;
越大,由H2C2O4·2H2O的质量分数表达式可知,其含量一定越大,B正确;
C.Fe元素的物质的量= ,若步骤I中KMnO4溶液不足,则步骤I中有一部分Fe2+没有被氧化,不影响V2的大小,则
,若步骤I中KMnO4溶液不足,则步骤I中有一部分Fe2+没有被氧化,不影响V2的大小,则![]() 不变,则对于测得Fe元素的含量无影响,C错误;
不变,则对于测得Fe元素的含量无影响,C错误;
D.结合C可知:若KMnO4溶液浓度偏低,则消耗KMnO4溶液的体积V1、V2均偏大,Fe元素的物质的量偏大,则测得样品中Fe元素含量偏高,D正确;
故答案为:![]() ;BD。
;BD。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】![]() 溶液与
溶液与![]() 溶液发生反应:
溶液发生反应:![]() ,达到平衡。下列说法不正确的是( )
,达到平衡。下列说法不正确的是( )
A. 加入苯,振荡,平衡正向移动
B. 经苯2次萃取分离后,在水溶液中加入![]() ,溶液呈血红色,表明该化学反应存在限度
,溶液呈血红色,表明该化学反应存在限度
C. 加入![]() 固体,平衡逆向移动
固体,平衡逆向移动
D. 该反应的平衡常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH→CH3COO+CH3CH2O+H2O
B. 醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2→Cu2++2H2O
C. 苯酚钠溶液中通入少量二氧化碳:2![]() +CO2+H2O
+CO2+H2O![]() 2
2![]() +CO
+CO![]()
D. 乙醛溶液与新制氢氧化铜碱性悬浊液共热CH3CHO+2Cu(OH)2+OH![]() CH3COO+ Cu2O↓+3H2O
CH3COO+ Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(主要成分为二硫化亚铁铜:CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为8CuFeS2+21O2 ![]() 8Cu+4FeO+2Fe2O3+16SO2 。
8Cu+4FeO+2Fe2O3+16SO2 。
(1)若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__________(填元素符号)。
(2)用稀H2SO4浸泡上述反应制取铜后剩余的固体残渣,取少量所得溶液,检验溶液中存在Fe3+的方法是_________(注明试剂、现象、结论)。
(3)上述冶炼过程产生大量SO2。下列处理方案中合理的是_____________(填代号)
a 高空排放 b 用于制备硫酸 c 用纯碱溶液吸收制Na2SO3 d 用浓硫酸吸收
(4)验证黄铜矿冶炼铜的反应后气体中含有SO2的方法是________________。
(5)实验室制备,收集干燥的SO2,所需仪器如下。
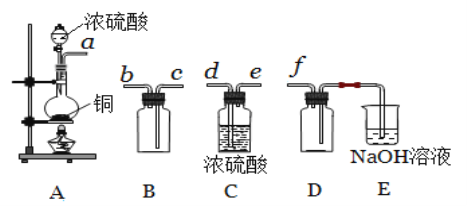
①其中装置A产生SO2 ,反应的化学方程式为_______________。
②请按气流方向连接各仪器接口,顺序为a →_____→_______→________→ _______→ f ,装置E中NaOH溶液的作用是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,某混合溶液中![]() ,1gc( CH3COOH)、1gc(CH3COO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。Ka为CH3COOH的电离常数,下列说法正确的是
,1gc( CH3COOH)、1gc(CH3COO-)、lgc(H+)和1gc(OH-)随pH变化的关系如下图所示。Ka为CH3COOH的电离常数,下列说法正确的是

A.O点时,![]()
B.N点时,![]()
C.该体系中,
D.pH由7到14的变化过程中, CH3COO-的水解程度始终增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.CaCO3与稀硝酸反应:![]()
B.FeSO4溶液与溴水反应:![]()
C.NaOH溶液与过量H2C2O4溶液反应:![]()
D.C6H5ONa溶液中通入少量CO2: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁与人类密切相关,几乎无处不在,地壳中大约5%是铁,是含量仅次于铝的金属.根据所学知识回答下列问题:
(1)铁原子价电子轨道表示式为______,与铁同周期的元素的基态原子中,最外层电子数与铁相同的元素共有_____种(包含铁)。
(2)下列关于铁的说法,不正确的是_____(填选项字母)
A.基态铁原子的电子排布式1s22s22p63s23p103d24s2违反了泡利原理
B.铁属于黑色金属,在周期表中属于ds区元素
C.铁丝可用于焰色反应实验时蘸取待测物,是由于铁在光谱图中无特征的谱线
D.Fe能与CO形成配合物Fe(CO)5,配体CO中C是配原子
(3)某铁的化合物结构简式如图所示。

①组成上述化合物中5种元素原子电负性由小到大的顺序为_____。
②上述化合物中氮原子的杂化方式有_____。
③在图中用“→”标出亚铁离子的配位键_____。
(4)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是后者,原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定CuSO4溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
Ⅰ.甲方案
实验原理:![]()
实验步骤:

(1)判断![]() 沉淀完全的操作为____________。
沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO4)=________molL-1。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO4)_________(填“偏高”、“偏低”或“无影响”)。
Ⅱ.乙方案
实验原理:![]() ,
,![]()

实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H2体积为bmL,已知实验条件下![]() ,则c(CuSO4)______molL-1(列出计算表达式)。
,则c(CuSO4)______molL-1(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO4)________(填“偏高”、“偏低”或“无影响”)。
(10)是否能用同样的装置和方法测定MgSO4溶液的浓度:_________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气(Cl2)是高中化学一种非常重要的气体单质,它是制备许多化工产品的原料。
Ⅰ.甲同学在实验室用体积比为1:3的氯气和空气(不参与反应)的混合气体与潮湿的碳酸钠反应来制备Cl2O,其实验装置如图所示。

已知:Cl2O熔点为-120.6℃,沸点为2.0℃,常温常压下为一种棕黄色气体。
(1)仪器B的名称为________,KMnO4与浓盐酸反应生成Cl2的离子方程式为________。
(2)装置C的作用为________,装置E中的现象是________。
(3)氯气与潮湿的碳酸钠制Cl2O的化学方程式为________。
Ⅱ.乙同学在实验室用Cl2和熔融的S反应制备S2Cl2,其实验装置如图所示。

已知:S2Cl2熔点为-76℃,沸点为138℃,常温下为橙黄色的液体,遇水易水解。
(4)W中盛放的试剂为________。
(5)乙同学应进行合理的操作顺序为________(填序号)。
a.点燃酒精灯 b.停止通氯气 c.开始通氯气 d.熄灭酒精灯
(6)检验S2Cl2和水反应的产生的气体为SO2的实验操作为________。
(7)本实验需改进的地方为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com