
Ⅰ.(1)某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a 。
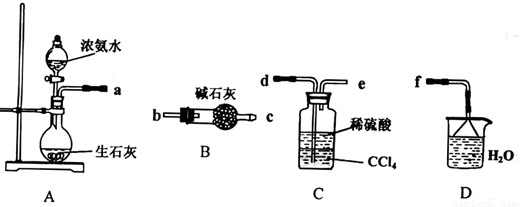
(2)将装置C中两种液体分离开的操作名称是___ __。装置D的作用是 。
Ⅱ.过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。工业上生产过氧化钙的主要流程如下:
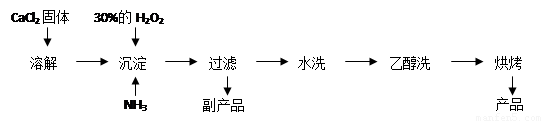
已知CaO2·8H2O呈白色,微溶于水。I2+2S2O32-= 2I-+S4O62-
(1)用上述方法制取CaO2·8H2O的化学方程式是 ;
(2)检验“水洗”是否合格的方法是 ;
(3)测定产品中CaO2的含量的实验步骤是:
第一步:准确称取a g产品于锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L—1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。
①判断此滴定实验达到终点的方法是: 。
②CaO2的质量分数为 (用字母表示);
Ⅰ(1)d e f (2分)
(2) 分液(2分) ;吸收多余的NH3防止污染空气,防止倒吸(2分)
Ⅱ(1)CaCl2+H2O2+2NH3+8H2O = CaO2·8H2O↓+2NH4Cl (2分)
(2)取最后一次洗涤液少许于试管中,再滴加稀硝酸酸化的硝酸银溶液,看是否产生白色沉淀。(2分)
(3)①当滴入最后一滴标准溶液时溶液由蓝色变为无色(或溶液褪色),且半分钟不变色
②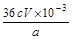 (2分)
(2分)
【解析】
试题分析:Ⅰ(1)A装置制备氨气,因为和硫酸溶液反应,不需要干燥,C装置可以防倒吸,长进短出,D装置用来吸收多余的氨气。接口顺序d e f;(2)两种溶液互不相溶,用分液漏斗来分离,D装置吸收多余的NH3防止污染空气,防止倒吸;Ⅱ根据流程图可以推出原料,结合质量守恒原理可以推断出方程式CaCl2+H2O2+2NH3+8H2O = CaO2·8H2O↓+2NH4Cl。水洗是为了除去沉淀表面的NH4Cl,最后检验氯离子即可,取最后一次洗涤液少许于试管中,再滴加稀硝酸酸化的硝酸银溶液,看是否产生白色沉淀;(3)CaO2把KI氧化为I2,加淀粉溶液为蓝色,当Na2S2O3把I2反应完之后溶液变为无色,所以滴定终点的判定是当滴入最后一滴标准溶液时溶液由蓝色变为无色(或溶液褪色),且半分钟不变色;②根据电子守恒CaO2---I2-----2 Na2S2O3,建立关系,可以推出质量分数。
2
? CV×10-3
考点:考查实验装置的连接、基本实验操作、方程式的书写、质量分数的计算


科目:高中化学 来源: 题型:
(6分)(1)某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,则该矿泉水中Mg2+的物质的量浓度为 .
(2)在KCl和CaCl2所组成的某混合物中,K+与Ca2+的物质的量之比为2∶1,则KCl与CaCl2的物质的量之比为 ,该混合物中CaCl2的质量分数为 .
查看答案和解析>>
科目:高中化学 来源:2010年辽宁省庄河市第六高级中学高一上学期第一次月考化学卷 题型:单选题
(6分)(1)某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,则该矿泉水中Mg2+的物质的量浓度为 .
(2)在KCl和CaCl2所组成的某混合物中,K+与Ca2+的物质的量之比为2∶1,则KCl与CaCl2的物质的量之比为 ,该混合物中CaCl2的质量分数为 .
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省高三上学期12月月考化学试卷(解析版) 题型:实验题
Ⅰ、 (1)某化学兴趣小组欲从下列装置中选取必要的装置制取 (NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a
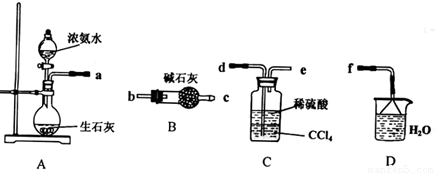
(2)将装置C中两种液体分离开的操作名称是__ _______。
装置D的作用是 。
Ⅱ、(4分)为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁(MgOHCl)的工艺。某同学根据该原理设计的实验装置如图:
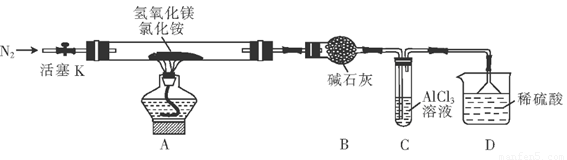
请回答下列问题:
(1) 装置A中发生反应生成碱式氯化镁的化学方程式为_________ ____
装置B中碱石灰的作用是_____ __
(2) 反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,二是_______________ ______
(3) 装置C的试管中反应的离子方程式为 ______________
查看答案和解析>>
科目:高中化学 来源:2010年辽宁省庄河市高一上学期第一次月考化学卷 题型:选择题
(6分)(1)某化学兴趣小组对“农夫山泉”矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,则该矿泉水中Mg2+的物质的量浓度为 .
(2)在KCl和CaCl2所组成的某混合物中,K+与Ca2+的物质的量之比为2∶1,则KCl与CaCl2的物质的量之比为 ,该混合物中CaCl2的质量分数为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com