
| A.氧气能转化成臭氧 | B.食盐水能导电 |
| C.钠能浮在水面上 | D.钾能溶于酒精 |
科目:高中化学 来源: 题型:
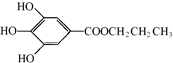 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.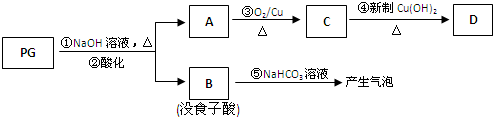
| △ |
| △ |


查看答案和解析>>
科目:高中化学 来源: 题型:
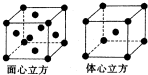
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 [化学--物质结构与性质]
[化学--物质结构与性质]查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
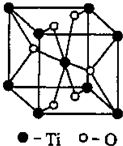 [化学-物质结构与性质]
[化学-物质结构与性质]查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省深圳市高三一模考试理综化学试卷(解析版) 题型:填空题
化合物G的合成路线如下:

(1)D中含氧官能团的名称为????? ??? ,1 mol G发生加成反应最多消耗????? ? mol H2
(2)除掉E中含有少量D的试剂和操作是?????? ;下列有关E的说法正确的是????? (填字母序号)。
A.可发生氧化反应
B.催化条件下可发生缩聚反应
C.可发生取代反应
D.是CH2=CHCOOCH2CH3的同系物
E.易溶于水
(3)写出A→B的化学反应方程式????????????????????????????? 。
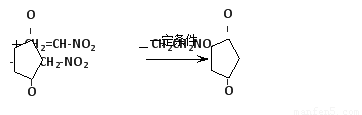
(4)反应E + F→ G属于下列麦克尔加成反应类型,则F的结构简式为?????? ??? 。
(5)比G少2个氢原子的物质具有下列性质:①遇FeCl3溶液显紫色;②苯环上的一氯取代物只有一种;③1mol物质最多可消耗2mol Na和1mol NaOH。任写一种该物质的结构简式????????? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com