
| A、甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
| B、常温下的溶液:KW/c(H+)=0.1mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C、稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| D、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢键属于共价键 |
B、因为分子间存在氢键的缘故,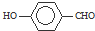 比 比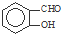 熔沸点高 熔沸点高 |
| C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D、1mol冰中有4mol氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某有机物A由C、H、O三种元素组成,在一定条件下有如下转化关系,己知在相同条件下,C的蒸气密度是氢气的22倍,并可以发生银镜反应.
某有机物A由C、H、O三种元素组成,在一定条件下有如下转化关系,己知在相同条件下,C的蒸气密度是氢气的22倍,并可以发生银镜反应.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、①③④⑤⑥ |
| C、②③⑥ | D、②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0mol?L-1的HNO3溶液:NH4+、[Ag(NH3)2]+、Cl-、SO42- |
| B、c(H+)/c(OH-)=10-11的溶液:Na+、Ba2+、NO3-、Cl- |
| C、滴入酚酞显红色的溶液:Ca2+、Al3+、NO3-、HCO3- |
| D、滴入碘化钾淀粉溶液显蓝色的溶液:Na+、Fe2+、ClO-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向氯化铝溶液中加入过量的氨水:3NH3?H2O+A13+═3NH4++Al(OH)3↓ |
| B、NaOH溶液吸收少量CO2:OH-+CO2═HCO3- |
| C、向氯化铁溶液中加入铜粉发生的反应:Cu+Fe3+═Cu2++Fe2+ |
| D、Na2O2与水的反应:Na2O2+H2O═2Na++2OH-+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com