
| 3 |
| 6 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
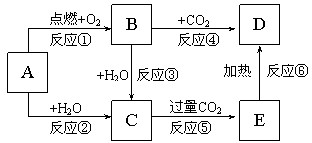 如图所示,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
如图所示,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.查看答案和解析>>
科目:高中化学 来源: 题型:
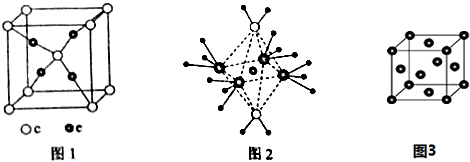
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.2 g |
| B、16.8 g |
| C、19.6 g |
| D、22.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜矿较易还原,铝矿很难还原 |
| B、铜矿颜色较深,易发现;铝矿颜色较浅,不易发现 |
| C、矿石在地下埋藏,铜矿最浅,容易开发,铝矿埋得深,难开发 |
| D、以上说法都是错误的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I2为氧化产物 |
| B、H2O2既作氧化剂又作还原剂 |
| C、氧化性强弱顺序为H2O2>I2 |
| D、生成1 mol I2时转移2 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从2L1mol?L-1的NaCl溶液中取出10 mL,其浓度仍是1 mol?L-1 |
| B、制成0.5L 1 mol?L-1的盐酸,需标准状况下氯化氢气体11.2 L |
| C、1L1mol?L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10g98%硫酸(密度为1.84g?cm-3)与10mL 18.4 mol?L-1硫酸的浓度是不同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
| B、常温下的溶液:KW/c(H+)=0.1mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C、稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| D、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com