
| 元素编号 | 相关信息 |
| U | 所处的周期数、族序数分别与其原子序数相等. |
| V | 基态时,电子分布在三个能级上,且各能级中电子数相等. |
| W | 基态时,2P轨道处于半充满状态 |
| X | 与W元素处于同一周期,且X第一电离能小于W的第一电离能 |


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、BaCl2+H2SO4=BaSO4↓+2HCl |
| B、Ba(OH)2+Na2SO4=BaSO4↓+2NaOH |
| C、Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 |
| D、Ba(OH)2+H2SO4=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
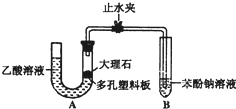
查看答案和解析>>
科目:高中化学 来源: 题型:
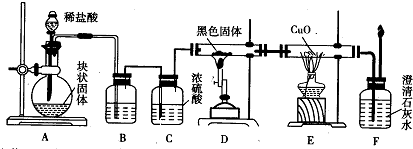
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
48 22 |
50 22 |
A、
| ||||
B、
| ||||
C、
| ||||
D、分别由
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 某研究性学习小组的同学在实验室对Cl2使有色物质褪色的机理进行了探究.
某研究性学习小组的同学在实验室对Cl2使有色物质褪色的机理进行了探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com