
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
A、电子式 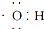 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
B、比例模型  可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 |
C、结构示意图为 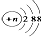 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 |
D、原子结构示意图 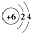 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤⑥⑦ | B、①④⑥⑦ |
| C、① | D、①④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
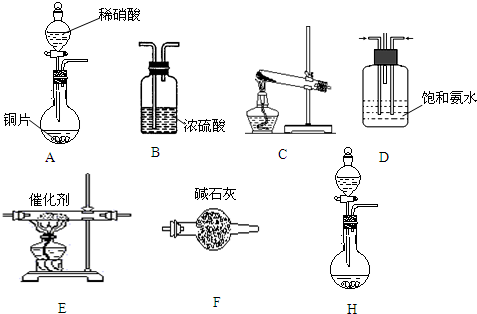
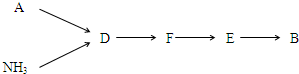
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 相关信息 |
| U | 所处的周期数、族序数分别与其原子序数相等. |
| V | 基态时,电子分布在三个能级上,且各能级中电子数相等. |
| W | 基态时,2P轨道处于半充满状态 |
| X | 与W元素处于同一周期,且X第一电离能小于W的第一电离能 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Na+、Cl- |
| B、K+、Na+、NO3-、CO32- |
| C、Na+、H+、NO3-、SO42- |
| D、Mg2+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
| B、醋酸溶液除水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、过氧化钠与水反应:2O22-+2H2O═4OH-+O2↑ |
| D、向NaAlO2溶液中滴加NaHCO3溶液HCO3-+AlO2-+H2O=A(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 预期现象与结论 |
| 步骤1:将适量稀H2SO4加入少许样品于试管中,加热溶解;然后将所得溶液分置 于A、B试管中. | 溶液呈黄绿色,说明溶液中含Fe2+或Fe3+. |
| 步骤2: | |
| 步骤3: | |
| … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com