
【题目】在唾液淀粉酶催化淀粉分解实验中,将唾液稀释10倍,与用唾液原液(没稀释)实验效果基本相同,这表明酶具有
A.专一性 B.稳定性
C.多样性 D.高效性
科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( )

A. 加热时,①中上部汇集了NH4Cl固体
B. 加热时,②中溶液变红,冷却后又都变为无色
C. 加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性
D. 三个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人工合成有机化合物H的路线可简单表示如图: 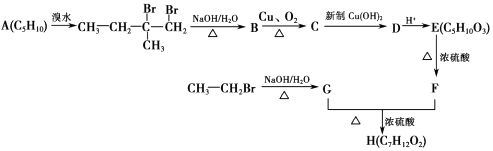 已知:F的核磁共振氢谱有四个峰,峰的面积比为1:1:3:3.
已知:F的核磁共振氢谱有四个峰,峰的面积比为1:1:3:3.
请回答下列问题:
(1)A的名称(系统命名)为;C中官能团的结构简式为 .
(2)G+F→H的反应类型为;H的结构简式为 .
(3)B→C的化学方程式为 .
(4)E→F的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.SF6是一种优良的绝缘气体,分子结构中,只存在S—F键,已知1 mol S(s)转化为气态硫原子吸收能量280 kJ,F—F键能为160 kJ·mol-1,S—F键能为330 kJ·mol-1,试写出S(s)和F2(g)反应生成SF6(g)的热化学方程式_______________________________。
Ⅱ.V、W、X、Y、Z是由四种短周期元素中的2种或3种组成的5种化合物,其中W、X、Z均由2种元素组成,X是导致温室效应的主要气体,Z是天然气的主要成分,Y、W都既能与酸反应,又能与强碱溶液反应。上述5种化合物涉及的四种元素的原子序数之和等于28;V由一种金属元素A和两种非金属元素B与C组成,其化学式构成为A(BC3)3 。它们之间的反应关系如下图:

(1)写出物质W的一种用途:__________________________________________________。
(2)写出V与足量NaOH溶液反应的化学方程式:________________________________。
(3)将少量的X通入某种物质的水溶液中可以生成Y,该反应的离子方程式为________________________________________________________________________。
(4)写出气体X的结构式__________。
(5)以Z为燃料,活性炭为电极,熔融碳酸盐(如熔融K2CO3)环境下制成燃料电池的负极反应式为_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:
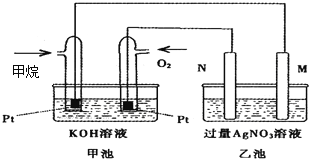
(1)M电极的材料是__________,其电极名称是_____________。
(2)N的电极反应式为____________________________,通入甲烷的电极反应式为______________________________________________,
(3)乙池总反应的化学方程式是_______________________________________________,
(4)在此过程中,乙池中某一电极析出金属银4.32g,甲池中理论上消耗氧气为_____mL(标准状况下),若此时乙池溶液的体积为400mL,则乙池中溶液的H+的浓度为__________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A与D是常见的有机化工原料,下列路线合成香料M(![]() ):
):

已知以下信息:
①A的相对分子质量为28
②2RCH2CHO![]()

(1)A的结构简式是________,D的名称是__________。
(2)A生成B的反应类型为_____________,G中官能团名称为___________。
(3)E生成F的的化学方程式为_________________________________________。
(4)下列关于G的说法正确的是______________。(填标号)
a.属于芳香烃
b.可与FeCl3溶液反应显紫色
c.1molG与H2完全加成,最多4molH2
d.可与新制的氢氧化铜共热生成红色沉淀
(5)化合物M的同系物N比M的相对分子质量大14,N的同分异构体中同时满足下列条件的共有__________种(不考虑立体构)。
①与化合物M含有相同的官能团; ②苯环上有两个邻位取代基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己二酸是一种重要的有机二元酸,能够发生成盐反应、酯化反应、酰胺化反应等,并能与二元胺或二元醇缩聚成高分子聚合物等,是合成尼龙-66的原料,工业上环己醇用硝酸氧化可得到己二酸,是典型的氧化还原反应。
 △H<0
△H<0
相关物理常数:
名称 | 相对分子质量 | 密度(20℃) g/cm3 | 熔点(℃) | 沸点(℃) | 溶解度S(g100g溶剂) | ||
水 | 乙醇 | 乙醚 | |||||
环己醇 | 100 | 0.96 | 25.2 | 161 | 可溶 | 易溶 | |
己二酸 | 146 | 1.36 | 151 | 265 | 可溶(S随温度降低而减小) | 易溶 | 微溶 |
I.己二酸粗产品的制备
操作步骤:装置C中加入50mL中等浓度的硝酸(过量),投入沸石,并逐一安 装装置A、装置B和温度计,磁力搅拌,将溶液混合均匀,并加热到80℃。用装置A滴加2滴环己醇,反应立即开始,温度随即上升到85~90℃,从装置A中小心地逐滴加入环己醇,将混合物在85-90℃下加热2-3 分钟,共加入1.000g环己醇。
请回答下列问题:

(1)反应需维持温度在85~90℃,最好采取______控温;试分析维持温度在85~90℃的原因:__________。
(2) 装置右侧烧杯中的NaOH 溶液的作用是:_______________。
II.己二酸粗产品的提纯及应用
操作流程:趁热倒出装置C 中的产品,在冷水中降温冷却,析出的晶体在布氏漏斗上进行抽滤,将晶体进行重结晶,再分别用3mL 冰水和乙醚洗涤己二酸晶体,继续抽滤,晶体再用3mL冰水洗涤一次,再抽滤。取出产品,干燥后称重,得干燥的己二酸0.860g。
请回答下列问题:
(3) 相比于普通过滤,抽滤的优点在于:_________
(4)在抽滤过程中,用冰水洗涤析出的己二酸晶体的原因:___________。
(5)该实验的产率为: _______% (结果保留3 位有效数字)
(6)工业上用己二酸与乙二醇反应形成链状高分子化合物,写出化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各图象的叙述,正确的是( ) 
A.甲图表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJmol﹣1
B.乙图表示恒温恒容条件下发生的可逆反应2NO2(g)N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙图表示
A.B两物质的溶解度随温度变化情况,将A,B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数仍为A%=B%D.丁图表示常温下,稀释HA,HB两种酸的稀溶液时,溶液的pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两电池电极材料都是铁棒与碳棒,请回答下列问题:

(1)若两电池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒.(填“Fe”或“C”)
②乙池中的阳极反应式为:________________.
③乙池中总反应的化学方程式为:________________.
(2)若两池中均为饱和NaCl溶液,溶液中滴两滴酚酞.
①乙池中总的离子方程式为:________________.
②甲池C极上的电极反应式为:________________.
③甲池中首先出现红色的是_____极;乙池中首先出现红色的是______极(填“Fe”或“C”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com