
【题目】下列有关实验方法正确的是( )
A.用铜片和浓硝酸反应制NO
B.加热NH4Cl和Ca(OH)2固体混合物制取NH3
C.用浓硫酸干燥NH3
D.用排水法收集NO2
【答案】B
【解析】A.Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,铜和浓硝酸反应生成二氧化氮,和稀硝酸反应生成NO,故A不符合题意;
B.2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O,故B符合题意;
CaCl2+2NH3↑+2H2O,故B符合题意;
C.氨水属于碱性气体,能和浓硫酸反应生成硫酸铵,所以要用碱石灰干燥氨气,故C不符合题意;
D.3NO2+H2O=2HNO3+NO,所以二氧化氮不能用排水法收集,应该采用向上排空气法收集,故D不符合题意;
所以答案是:B.
【考点精析】关于本题考查的氨的实验室制法,需要了解安验室制法:用铵盐与碱共热,2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O才能得出正确答案.


科目:高中化学 来源: 题型:
【题目】从化学键的角度看化学反应的实质是“旧化学键的断裂,新化学键的形成”,下列既有旧化学键的断裂,又有新化学键的形成的变化是
A.碘升华B.Cl2 溶于水C.氯化钠受热熔化D.酒精溶解于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W、X、Y、Z原子的最外层电子数之和为21,下列说法中不正确的是
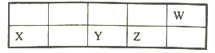
A. 原子半径:X>Y>W
B. 简单阴离子的还原性:Z>W
C. 气态氢化物的稳定性:W>Y
D. 氧化物对应水化物的酸性:Z>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】提供如下试剂:烧碱、铜片、大理石、蒸馏水,欲进行以下物质的制取或实验,从欠缺试剂的角度看,无法进行的是( )
A.制取纯碱B.制取氧化铜
C.测定烧碱的物质的量D.制取氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴是制备钴的氧化物的重要原料。下图为二水合草酸钴(CoC2O4·2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。
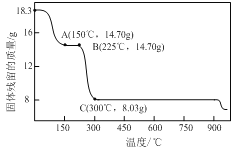
①通过计算确定C点剩余固体的化学成分为________(填化学式);试写出B点对应的物质与O2在225℃~300℃发生反应的化学方程式:_______________________________________________;
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物体生命活动的主要承担者、遗传信息的携带者、结构和功能的基本单位、生命活动的主要能源物质依次是 ( )
A.核酸、蛋白质、细胞、糖类 B.蛋白质、核酸、细胞、脂肪
C.蛋白质、核酸、细胞、糖类 D.核酸、蛋白质、糖类、细胞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废液里含有FeCl2、CuCl2和FeCl3 . 为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程: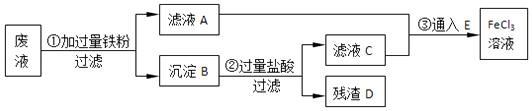
(1)A的化学式为 , E的化学式为 .
(2)B的化学成份 , 回收的铜是(填A、B、C、D或E).
(3)根据图示,反应②的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铅(Pb3O4,也可写作2PbO·PbO2)俗名“铅丹”或“红丹”,可用作防锈剂。工业上以废旧铅酸电池的铅膏(主要成分是PbSO4和PbO2)为原料制备Pb3O4的流程如下:
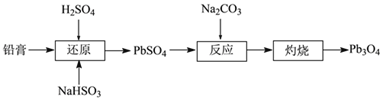
(1)“还原”时的化学方程式为________。
(2)已知:Ksp[PbCO3]=1.5×10-13。若使溶液中Pb2+的浓度小于1×10-5 molL-1,此时溶液中的c(CO32-) > ________molL-1。
(3)为测定某样品四氧化三铅含量,称取样品0.1200g,加入足量的6 molL-1HNO3充分溶解,过滤,得到含Pb2+的滤液和PbO2固体。将固体PbO2连同滤纸一并置于另一只锥形瓶中,加入足量的醋酸和醋酸钠混合溶液,再加入过量KI,使PbO2充分氧化I-,以淀粉溶液作指示剂,用0.01000molL-1 Na2S2O3溶液滴定,终点时用去30.00 mL。已知:I2 + 2Na2S2O3 = Na2S4O6 + 2NaI。
①所加KI必须过量,原因是________。
②计算试样中Pb3O4的质量分数_____。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】膜技术原理在化工生产中有着广泛的应用,有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,装置图如下。下列说法不正确的是
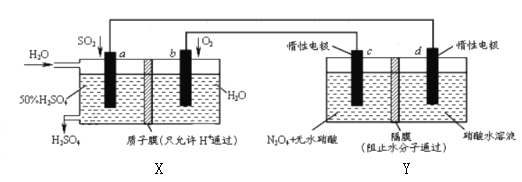
A. X是原电池,能够生产硫酸;Y是电解池,能够生产N2O5
B. C电极的电极反应方程式为N2O4+2HNO3-2e-=2N2O5+2H+
C. 当电路中通过2mole,X、Y中各有2molH+从左边迁移到右边
D. 电路中电子流向为a![]() d
d![]() c
c![]() b
b![]() a形成闭合回路
a形成闭合回路
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com