
【题目】现有下列九种物质:①盐酸 ②石墨 ③蔗糖 ④CO2 ⑤熔融NaHSO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧硫酸 ⑨明矾
(1)属于电解质的有_________________________;
属于非电解质的有__________________________;
能导电的物质有____________________________。
(2)②和SiO2在高温下可发生如下反应:
3C+SiO2![]() SiC+2CO
SiC+2CO
上述反应中还原产物是 ;氧化剂与还原剂物质的量之比为 。
(3)上述九种物质中有两种物质之间可发生离子反应:H++OH-===H2O,该离子反应对应的化学方程式为________________________
(4)⑤的电离方程式为______________________。
【答案】
(1)⑤⑥⑧⑨ ③④ ①②⑤⑦
(2) SiC 1:2(2分)
(3)Ba(OH)2+2HCl=BaCl2+2H2O(2分)
(4)NaHSO4=Na++HSO4-(2分)
【解析】
试题分析:①盐酸是溶液,不是电解质,也不是非电解质,但能导电;②石墨是单质,不是电解质,也不是非电解质,但能导电; ③蔗糖是非电解质,也不能导电;④CO2是非电解质,也不能导电;⑤熔融NaHSO4是电解质,能导电;⑥Ba(OH)2固体是电解质,不能导电;⑦氨水是溶液,不是电解质,也不是非电解质但能导电;⑧硫酸是电解质,但不能导电;⑨明矾是电解质,但不能导电;
(1)属于电解质的有⑤⑥⑧⑨;属于非电解质的有③④;能导电的物质有①②⑤⑦;
(2)在3C+SiO2![]() SiC+2CO碳既是氧化剂,又是还原剂,反应中还原产物是SiC;氧化剂与还原剂物质的量之比为1:2;
SiC+2CO碳既是氧化剂,又是还原剂,反应中还原产物是SiC;氧化剂与还原剂物质的量之比为1:2;
(3)上述九种物质中盐酸和氢氧化钡反应可发生离子反应:H++OH-===H2O,Ba(OH)2+2HCl=BaCl2+2H2O;
(4)熔融时共价键不破坏,只破坏离子键,熔融NaHSO4的电离方程式为NaHSO4=Na++HSO4-。


科目:高中化学 来源: 题型:
【题目】能用键能大小解释的事实是
A. 稀有气体化学性质很稳定 B. 硝酸易挥发,而硫酸难挥发
C. 氮气的化学性质比氧气稳定 D. 常温常压下,溴呈液态,碘呈固态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化石墨烯(结构如图所示)是一种性能优异的新型碳材料。实验室制备氧化石墨烯的一种方法如下:

(1)将浓硫酸“冷却至0℃”可采用的方法是 。
(2) 步骤②采用100目鳞片状的石墨,其主要目的是 ;图示的“搅拌”方式为 。
(3)步骤③④中加NaNO3和KMnO4的作用是 。
(4)步骤⑧H2O2还原剩余的KMnO4反应的离子方程式为 ;检验洗涤已无SO42-的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学--选修物质结构与性质】
信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门。
信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为﹣96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)写出Fe(26号元素)原子的基态电子排布式为 。
(2)CH3COCH3分子中含有 个π键,含有 个δ键。
(3)固态氯化铬酰属于 晶体,丙酮中碳原子的杂化方式为 ,二硫化碳属于 (填极性”或“非极性”)分子。
(4)K[Cr(C2O4)2(H2O)2]也是铬的一种化合物,该化合物属于离子化合物,其中除含离子键、共价键外,还含有有 键。
(5)金属铬的晶胞如下图所示,一个晶胞中含有 个铬原子。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①某NaCl样品中可能含有SO42-、CO32-,为检验杂质离子的存在,采取如下实验步骤:
样品![]() 无明显现象
无明显现象![]() 无明显现象。
无明显现象。
则加入的试剂A为 ,B为 (填化学式),该现象证明样品中不含有 。
②在后续实验中需要使用450mL0.5 mol·L-1NaCl溶液,为配制该浓度NaCl溶液进行实验,需用托盘天平称取NaCl g。
③配制NaCl溶液时,若出现下列操作,会使配制浓度偏高的是( )
A.称量时NaCl已潮解 |
B.天平砝码已锈蚀 |
C.定容时俯视刻度线 |
D.定容摇匀后液面下降,又加水至刻度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. υ(A)=0.5mol/(L·s) B. υ(B)=0.3mol/(L· s) C. υ(C)=0.8mol/(L·s) D. υ(D)=1mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水热法制备Fe2O3纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,关于该反应下列说法正确的是
A.H2O和S4O62-都是还原产物
B.1molFe2+参加反应时,转移2mol电子
C.Fe2+、S2O32-都是还原剂
D.x=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制备七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:
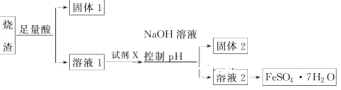
下列说法不正确的是
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定有SiO2,控制pH是为了使Al3+转化为Al(OH)3进入固体2
C.从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com