
 2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )。
2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )。
| A.点a的正反应速率比点b的小 |
| B.点c处反应达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D.其他条件不变,773 K下反应至t1时刻,n(H2)比上图中d点的值大 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
 NaOH+H2↑+Cl2↑(未配平),该反应中NaCl的电子式是______;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐______t。(可能用到的相对原子质量:Na:23,Cl:35.5,H:1,O:16)
NaOH+H2↑+Cl2↑(未配平),该反应中NaCl的电子式是______;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐______t。(可能用到的相对原子质量:Na:23,Cl:35.5,H:1,O:16)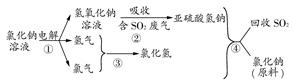
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制普通玻璃的主要原料是纯碱、石灰石、石英 |
| B.氨是制作氮肥、硝酸、铵盐的重要原料 |
| C.将二氧化硫催化氧化生成三氧化硫后,在吸收塔内用水吸收制得浓硫酸 |
| D.制造普通水泥的主要原料是黏土、石灰石 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2合成SO3虽然属于放热反应,但工业上合成SO3时仍需加热 |
| B.合成氨工业采用高温高压和使用催化剂,因这些条件都符合化学平衡原理 |
| C.合成纯碱的过程中,应首先向饱和食盐水中通入NH3,再通入足量CO2 |
| D.通过加压降温的方法可获得制备NH3的原料气N2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使用铁触媒,使平衡向生成NH3的方向移动 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.500 ℃左右比室温更有利于合成氨的反应 |
| D.合成氨时采用循环操作可提高原料的利用率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
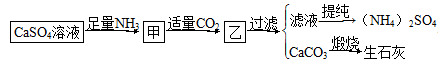
| A.往甲中通CO2有利于(NH4)2SO4生成 |
| B.生成1 mol(NH4)2SO4至少消耗2 mol NH3 |
| C.在实际生产中CO2可被循环使用 |
| D.直接蒸干滤液能得到纯净的(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)(正反应为放热反应),下列说法中正确的是( )。
2NH3(g)(正反应为放热反应),下列说法中正确的是( )。| A.达到平衡后加入N2,当重新达到平衡时,NH3的浓度比原平衡的大,H2的浓度比原平衡也大 |
| B.达到平衡后,升高温度,既加快了正、逆反应的速率,又提高了NH3的产率 |
| C.达到平衡后,缩小容器的体积,既有利于加快正、逆反应速率,又有利于提高氢气的转化率 |
| D.加入催化剂可以缩短达到平衡的时间,是因为正反应速率增大了,逆反应速率减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
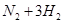


 。
。

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 下列分析中正确的是
下列分析中正确的是| A.变质的植物油有难闻的特殊气味,是山于植物油发生了水解反应 |
| B.某雨水样品放置一段时间后pH由4.68变为4.00,是因为水中溶解的CO2增多 |
| C.氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性 |
| D.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com