
【题目】咖啡酸具有止血功效,存在于多种中药中,其结构简式如图。
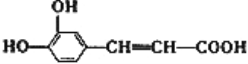
(1)写出咖啡酸中两种含氧官能团的名称:____________。
(2)根据咖啡酸的结构,列举咖啡酸非含氧官能团可以发生的二种反应类型:____________。
(3)蜂胶的分子式为C17H16O4,在一定条件下可水解生成咖啡酸和一种醇A,则醇A的分子式为________。
(4)已知醇A含有苯环,且分子结构中无甲基,写出醇A在一定条件下与乙酸反应的化学方程式:
____________________________________________________。
【答案】羧基、羟基 加成反应,加聚反应,氧化反应 C8H10O CH3COOH+![]()
![]()
![]() +H2O
+H2O
【解析】
(l)由图中咖啡酸的结构简式可知,该物质含有酚羟基、羧基和碳碳双键,其中含氧官能团为羧基、羟基;答案:羧基、羟基。
(2) 由图中咖啡酸的结构简式可知,该物质含有的非氧官能团是碳碳双键,碳碳双键可以发生加聚反应,加成反应和氧化反应;答案:加成反应,加聚反应,氧化反应
(3) 蜂胶的分子式为C17H16O4,在一定条件下可水解生成咖啡酸和一种醇A,利用原子守恒规律,咖啡酸的结构简式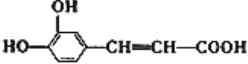 ,分子式为C9H804,可求出A的分子式C8H10O;答案:C8H10O。
,分子式为C9H804,可求出A的分子式C8H10O;答案:C8H10O。
(4) 因为醇A含有苯环,且分子结构中无甲基,符合题意的醇A为![]() ,与乙酸发生酯化反应的化学方程式:CH3COOH+
,与乙酸发生酯化反应的化学方程式:CH3COOH+![]()
![]()
![]() +H2O。答案:CH3COOH+
+H2O。答案:CH3COOH+![]()
![]()
![]() +H2O。
+H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】As和P属于同主族元素,它们都能形成多种含氧酸。中国自古就有“信口雌黄”“雄黄入药”之说。雌黄(As2S3)和雄黄(As4S4)早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。在一定条件下,雌黄和雄黄的转化关系如图所示。

(1)亚磷酸(H3PO3)是一种精细化工产品。亚磷酸(H3PO3)与足量NaOH溶液反应生成Na2HPO3。
①则亚磷酸为___(填“一”“二”或“三”)元酸。
②查阅资料知25℃时,亚磷酸(H3PO3)的Ka1=5×10-2,Ka2=2.5×10-7,Na2HPO3可使碘水褪色,25℃时,Na2HPO3水解反应的Kh=____,若向Na2HPO3溶液中加入少量的I2,则溶液中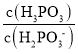 将__(填“增大”、“减小”或“不变”)
将__(填“增大”、“减小”或“不变”)
(2)反应II中,若0.5molAs4S4参加反应,转移14 mol电子,则物质a为__(填化学式)
(3)反应Ⅲ中的产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态。常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化如图所示。
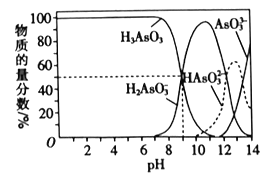
以酚酞为指示剂,将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为红色时停止滴加。该过程中主要反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜和浓硫酸可以在加热条件下发生反应,化学方程式如下(已配平):Cu+2H2SO4![]() CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:
CuSO4+A↑+2H2O,试通过计算和推理完成下面的问题:
(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为___。A物质可以与强碱反应生成盐和水。则A应该属于___(用字母代号填写)。
A.酸 B.酸性氧化物 C.盐 D.电解质 E.非电解质
(2)一定量的铜片与含1.2mol的H2SO4的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.4mol电子,生成的A气体在标况下的体积为___L(假设气体全部逸出)。
(3)将(2)中反应后所得的溶液稀释后与足量的Ba(OH)2溶液反应,所得沉淀的质量为___g。写出此过程中发生反应的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数![]() (X)随pH的变化如图所示[已知
(X)随pH的变化如图所示[已知![]() (X) =
(X) =![]() ]。下列叙述错误的是( )
]。下列叙述错误的是( )

A. pH=1.2时,c(K+)+c(H+)=c(H2A)+c(OH-)
B. 常温下,H2A的电离平衡常数Ka2=10-42
C. pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D. KHA溶液中离子浓度为c(K+)>c(HA-)>c(OH-)>c(H2A)>c(H+)>c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铬(CrN)是一种良好的耐磨材料,实验室可用无水氯化铬(CrCl3)与氨气在高温下反应制备,反应原理为CrCl3+NH3![]() CrN+3HCl.回答下列问题:
CrN+3HCl.回答下列问题:
(1)制备无水氯化铬。氯化铬有很强的吸水性,通常以氯化铬晶体(CrCl3·6H2O)的形式存在。直接加热脱水往往得到Cr2O3,有关反应的化学方程式为______________,以氯化铬晶体制备无水氯化铬的方法是_____________________________。
(2)制备氮化铬。某实验小组设计制备氮化铬的装置如下图所示(夹持与加热装置省略):
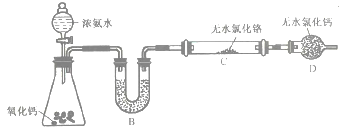
①装置A中发生反应的化学方程式为_____________________。
②实验开始时,要先打开装置A中活塞,后加热装置C,目的是___________________。
③装置B中盛放的试剂是____________,装置D的作用是_____________________。
④有同学认为该装置有一个缺陷,该缺陷是_______________________。
(3)氯化铬的纯度测定。制得的CrN中含有Cr2N杂质,取样品14.38g在空气中充分加热,得固体残渣(Cr2O3)的质量为16.72g,则样品中CrN的质量分数为_____________(结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷和丙烷的混合气体完全燃烧后,先将产物通过浓硫酸,浓硫酸增重3.06g,然后通过Na2O2,Na2O2增重3.36g。混合气体中乙烷和丙烷的体积比为
A. 1:1B. 2:3C. 3:2D. 3:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某仅含碳、氢、氧三种元素组成的有机化合物的结构,进行了如下实验。首先取该有机化合物样品4.6 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重5.4 g和8.8 g;然后用质谱仪测定其相对分子质量,经测定得到如图1所示的质谱图;最后用核磁共振仪处理该有机物,得到如图2所示的核磁共振氢谱图。

试回答下列问题:
(1)该有机化合物的相对分子质量为___________;
(2)该有机物的实验式为___________;
(3)能否根据该有机物的实验式确定其分子式___________ (填“能”或“不能”),原因是___________,该有机化合物的分子式为___________。
(4)请写出该有机化合物的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,反应![]() +H2O
+H2O![]() H2CO3+OH的平衡常数K=2.2×108。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
H2CO3+OH的平衡常数K=2.2×108。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
A. 0.2mol·L1氨水:c(NH3·H2O)>c(![]() )>c(OH)>c(H+)
)>c(OH)>c(H+)
B. 0.2mol·L1NH4HCO3溶液(pH>7):c(![]() )>c(
)>c(![]() )>c(H2CO3)>c(NH3·H2O)
)>c(H2CO3)>c(NH3·H2O)
C. 0.2mol·L1氨水和0.2mol·L1NH4HCO3溶液等体积混合:c(![]() )+c(NH3·H2O)=c(H2CO3)+c(
)+c(NH3·H2O)=c(H2CO3)+c(![]() )+c(
)+c(![]() )
)
D. 0.6mol·L1氨水和0.2mol·L1NH4HCO3溶液等体积混合:c(NH3·H2O)+c(![]() )+c(OH)=0.3mol·L1+c(H2CO3)+c(H+)
)+c(OH)=0.3mol·L1+c(H2CO3)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 有机物(![]() )的名称为2-甲基-1-丙醇
)的名称为2-甲基-1-丙醇
B. 芥子醇( )能发生氧化、取代、水解、加聚反应
)能发生氧化、取代、水解、加聚反应
C. 1mol绿原酸( )与足量溴水反应,最多消耗4molBr2
)与足量溴水反应,最多消耗4molBr2
D. 有机物(俗称“一滴香”)( )的一种含苯环的同分异构体能发生银镜反应
)的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com