
【题目】[化学——选修5:有机化学基础]
氯贝特(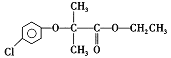 )是临床上一种抗血栓药物,它的一种合成路线如图28(图中部分反应条件及部分反应物、生成物已略去)。
)是临床上一种抗血栓药物,它的一种合成路线如图28(图中部分反应条件及部分反应物、生成物已略去)。
回答下列问题: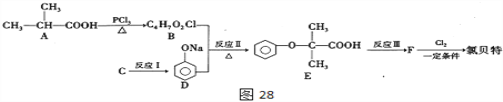
(1)有机物A命名为________,反应II的反应类型为_________,E分子中含有的官能团名称是___________。
(2)要实现反应I的转化,加入下列物质能达到目的有__________。
a. NaHCO3 b. NaOH c.Na2CO3 d. CH3COONa
(3)写出反应Ⅲ的化学方程式__________________________________ 。
(4)产物E有多种同分异构体,满足下列条件的所有同分异构体G有______种。
① 属于酯类且与FeCl3溶液显紫色 ② 能发生银镜反应
③ 1molG最多与2molNaOH反应 ④ 苯环上只有2个取代基且处于对位
其中核磁共振氢谱有五组峰的有机物结构简式为______________________。
(5)结合以上合成路线信息,设计以CH3CH2COOH为原料(无机试剂任选),合成有机物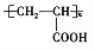 的合成流程。____________
的合成流程。____________
【答案】 2-甲基丙酸(或甲基丙酸) 取代反应 醚键、羧基 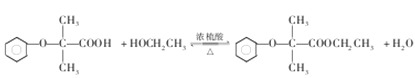 b、c
b、c 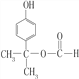 5
5 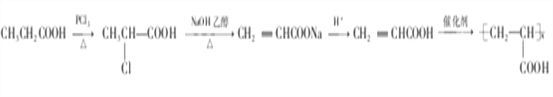
【解析】有机物A:(CH3)2CHCOOH发生信息反应生成的B为ClC(CH3)2COOH,C反应得到D为苯酚钠,则C应为苯酚;由氯贝特的结构可知E与乙醇反应生成F为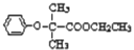 ;
;
(1)有机物(CH3)2CHCOOH命名为2-甲基丙酸(或甲基丙酸),B和D反应生成E的反应类型为取代反应, 分子中含有的官能团名称是醚键、羧基;
分子中含有的官能团名称是醚键、羧基;
(2)要实现苯酚与苯酚钠的转化,可结合苯酚的弱酸性,酸性比HCO3-强,比碳酸、醋酸弱,可分别与NaOH、Na或Na2CO3反应生成苯酚钠,即答案为b、c;
(3)反应Ⅲ的化学方程式为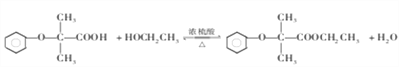 ;
;
(4)① 属于酯类且与FeCl3溶液显紫色,说明既有酯基又有酚羟基;② 能发生银镜反应,说明含有醛基或甲酸酯基;③1molG最多与2molNaOH反应,除去酚羟基与NaOH反应外,说明1mol酯基水解只消耗1molNaOH;④ 苯环上只有2个取代基且处于对位,说明除酚羟基外,另一个基团是HCOO-C3H6—,此基团的可能结构有HCOOCH2CH2CH2—、HCOOCH(CH3)CH2—、HCOOCH2CH(CH3)—、HCOOC(CH3)2—、HCOOCH(C2H5)—,共5种;其中核磁共振氢谱有五组峰的有机物结构简式为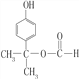 ;
;
(5)以CH3CH2COOH为原料,合成有机物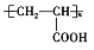 的合成流程为
的合成流程为 。
。


科目:高中化学 来源: 题型:
【题目】我们利用物质的结构与性质对周期表进行研究,有助于我们更好地掌握同类知识。
(1)基态砷原子中,价电子占用_________个原子轨道;雌黄分子式为As2S3,分子结构如图,则As原子的杂化方式为_________ 。

(2)N2与CO互为等电子体,则1molCO分子中含有的π键数目是_________个。
(3)向CuSO4溶液中加人少量氨水生成蓝色沉淀,继续加人过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加人一定量乙醇,析出[Cu(NH3)4]SO4 .H2O晶体;该晶体所含的非金厲元素中,N、O、S第一电离能由大到小的顺序是_________ (填元素符号),SO42-的空间构型为____________,晶体中含有的化学键有__________。加人乙醇后析出[Cu(NH3)4]SO4 .H2O晶体的原因是____________。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如下左图所示,由A、B两种微粒构成。 将其加热至148℃熔化,形成一种能导电的熔体。已知A微粒与CCl4具有相同的空间构型和相似的化学键特征,则A为_________ , B为_______________。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,下右图为其立方晶胞。已知晶体中最近的硼原子和磷原子核间距为x cm,磷化硼的摩尔质量为bg.·mol-1,阿伏加德罗常数为NA,则磷化硼晶体密度的表达式
为____________g.cm-3。(列出计算式即可)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 化石燃料在任何条件下都能充分燃烧
B. 化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体
C. 直接燃烧煤不如将煤进行深加工后,再燃烧效果好
D. 固体煤变为气体燃料后,燃烧效率将更低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于二氧化硅的叙述不正确的是
① 二氧化硅是制造光导纤维的重要原料
② 硅、碳原子最外层都有4个电子,故SiO2的物理性质与CO2类似
③ SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,是两性氧化物
④ 将CO2通入Na2SiO3溶液中有胶状沉淀生成,说明碳酸比硅酸酸性强
A. ②③ B. ③④ C. ②④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生产和生活中有广泛的应用。
Ⅰ、高铁酸钠(Na2FeO4)是一种新型净水剂,工业上制备高铁酸钠的反应原理为:
Fe(OH)3 + NaClO + NaOH →Na2FeO4 + X + H2O(未配平), 则X的电子式为_______ ,反应中被氧化的物质是_________(写化学式)。
Ⅱ、铁红颜料跟某些油料混合,可以制成防锈油漆。工业制硫酸产生的硫酸渣中主要含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
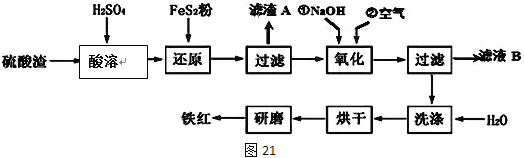
已知:
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
已知FeS2是一种黄色难溶于水的固体。
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为______________________;
“滤渣A”主要成份的化学式为__________________。
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,写出该反应的离子方程式_________________。
(3)为确保铁红的质量和纯度,氧化过程中加NaOH调节溶液pH的范围是____;如果加NaOH调节溶液pH=a,则滤液B中c(Fe3+)=____mol/L(25℃时,Ksp[Fe(OH)3]=4×10﹣38)
(4)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可以构成燃料电池。该电池负极的电极反应式为________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 光导纤维的主要成分为二氧化硅 B. SiO2是酸性氧化物,它不溶于任何酸
C. SiO2的俗名叫水玻璃,不溶于水 D. Si在自然界中既有游离态又有化合态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲乙丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):N2(g)+3H2(g)![]() 2NH3(g) △H<0,相关数据如下表所示:
2NH3(g) △H<0,相关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | lmol N2、3molH2 | 2mol NH3 | 2mol NH3 |
平衡时容器体积 | V甲 | V乙 | V丙 |
反应的平衡常数K | K甲 | K乙 | K丙 |
平衡时NH3的浓度/mol ·L-1 | C甲 | C乙 | C丙 |
平衡时NH3的反应速率/mol·L-1·min-1 | v甲 | V乙 | V丙 |
下列说法正确的是
A. V甲>V丙 B. C乙>C甲 C. K乙> K丙 D. V甲= V丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是

A. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
B. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol电子
3H2+CO,每消耗1molCH4转移12mol电子
C. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
D. 电池工作时,CO32-向电极B移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质之间的转化关系如图所示(部分产物已略去),下列说法正确的是( )
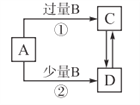
A. 若A为AlCl3溶液,B可能为氨水,反应①的离子方程式为:A13++4NH3·H2O=AlO2+ 4NH4++2H2O
B. 若A为Fe,B可能为稀硝酸,反应②的离子方程式为: 3Fe+8H++2NO3=3Fe2++2NO↑+4H2O
C. 若A为NaOH溶液,B可能为CO2,可用Ca(OH)2溶液鉴别C、D溶液
D. 若A为Cl2,B可能为NH3,实验室可用加热固体C的方法制取NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com