
【题目】某盐溶液NaHR的电离方程式为NaHR=Na++HR-下列有关说法不正确的是
A.Na2R溶液的pH值一定大于7
B.若NaHR溶液中c( OH-)>c( R2-)则溶液呈碱性
C.c(Na+)>c(HR-)>c( R2-)>c(OH-)>c( H+)
D.NaHR溶液的pH值不一定大于7
【答案】C
【解析】
A.根据某盐溶液NaHR的电离方程式为NaHR=Na++HR-,可知H2R为二元弱酸,则Na2R在溶液中能水解;
B.HR-在溶液中存在电离平衡和水解平衡,根据二者的程度判断溶液的酸碱性;
C.若c( R2-)>c(OH-),以电离为主,溶液呈酸性;
D.不能确定HR-在溶液中是以电离为主还是水解为主,则不能确定溶液的酸碱性。
A.根据某盐溶液NaHR的电离方程式为NaHR=Na++HR-,可知H2R为二元弱酸,则Na2R在溶液中能水解使溶液显碱性,所以Na2R溶液的pH值一定大于7,A正确;
B.HR-在溶液中存在电离平衡和水解平衡,HR-+H2O![]() OH-+H2R,HR-
OH-+H2R,HR-![]() H++R2-,若NaHR溶液中c(OH-)>c( R2-),则水解程度大于电离程度,所以溶液显碱性,B正确;
H++R2-,若NaHR溶液中c(OH-)>c( R2-),则水解程度大于电离程度,所以溶液显碱性,B正确;
C.HR-在溶液中存在电离平衡和水解平衡:HR-![]() H++R2-,HR-+H2O
H++R2-,HR-+H2O![]() OH-+H2R,若c( R2-)>c(OH-),以电离为主,溶液呈酸性,则c(Na+)>c(HR-)>c( H+)>c( R2-)>c(OH-),错误;
OH-+H2R,若c( R2-)>c(OH-),以电离为主,溶液呈酸性,则c(Na+)>c(HR-)>c( H+)>c( R2-)>c(OH-),错误;
D.HR-在溶液中存在电离平衡和水解平衡:HR-![]() H++R2-,HR-+H2O
H++R2-,HR-+H2O![]() OH-+H2R,若HR-在溶液中是以电离为主,则溶液显酸性,若以水解为主,则溶液显碱性,所以NaHR溶液的pH值不一定大于7,D正确;
OH-+H2R,若HR-在溶液中是以电离为主,则溶液显酸性,若以水解为主,则溶液显碱性,所以NaHR溶液的pH值不一定大于7,D正确;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应3A(g)+2B(g) ![]() 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是( )
A. 该反应的化学平衡常数表达式是![]()
B. 此时,B的平衡转化率是40%
C. 增大该体系的压强,化学平衡常数增大
D. 增加B,B的平衡转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是CO2催化还原为CH4示意图。下列说法不正确的是( )
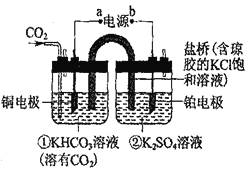
A.该过程是电能转化为化学能的过程
B.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O
C.一段时间后,①池中n(KHCO3)不变
D.一段时间后,②池中溶液的pH一定下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)下表是25℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为__。
(2)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是(填“>”、“<”或“=”):CH3COOK_____NaClO,两溶液中:[c(Na+)-c(ClO-)]_____[c(K+)-c(CH3COO-)]。
(3)碳酸钠溶液中滴加少量氯水的离子方程式为__________。
(II)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

(4)写出阳极的电极反应式_________。
(5)分析产品室可得到H3PO2的原因___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知AgCl的Ksp=1.8×10-10。常温下在100 mL 0.01 mol·L-1 KCl溶液中,加入1 mL0.01 mol·L-1 AgNO3溶液,下列说法正确的是 ( )
A.有AgCl沉淀析出B.无AgCl沉淀析出
C.无法确定D.有沉淀但不是AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
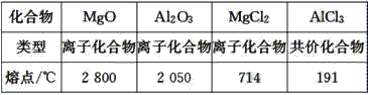
工业制镁时,电解MgCl2而不电解MgO的原因是__________________________________;
制铝时,电解Al2O3而不电解AlCl3的原因是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
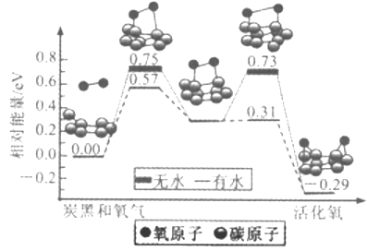
A. 氧分子的活化包括O-O键的断裂与C-O键的生成
B. 每活化一个氧分子放出0.29eV的能量
C. 水可使氧分子活化反应的活化能降低0.42eV
D. 炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向浓度为0.1 mol·L-1、体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。据图信息回答:
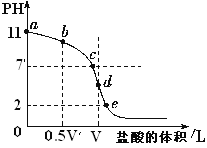
(1)该温度时NH3·H2O的电离常数K=________。
(2)比较b、c、d三点时的溶液中,由水电离出的c(OH-)大小顺序为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯的叠氮酸(HN3)是一种弱酸,常温下向25mL 0.1 mol/L NaOH溶液中加入0.2 mol/L HN3溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如下图。下列说法正确的是( )
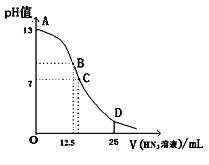
A. 该滴定过程中应用甲基橙作指示剂
B. 若B点pH=8,则c(HN3)=(10-6~10-8 )mol/L
C. 点D对应溶液中存在关系:c(HN3)>c(Na+)>c(N3-)
D. 沿曲线A→B→C的过程中,由水电离产生的c(OH-)逐渐减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com