
【题目】铜是人类发现最早并广泛使用的一种金属。溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I-=2CuI↓+![]()
②![]() +2
+2![]() =
=![]() +3I-
+3I-
现取某20.00mL含Cu2+的溶液。加入足量的KI充分反应后,用0.1000mo1·L-1的Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积如表所示。
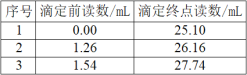
(1)溶液中Cu2+的浓度为___mol·L-1。
(2)用移液管量取20.00mLCu2+的溶液时俯视刻度线,最终测得的Cu2+的浓度将___(“偏高、偏低或无影响”)。
【答案】0.1250mol·L-1 偏低
【解析】
根据反应的方程式得出关系式计算铜离子浓度;根据俯视刻度线读数偏小分析误差。
(1)根据表中数据三次实验消耗Na2S2O3溶液体积分别是25.10mL、24.90mL、26.20mL,第三次实验误差大,舍去,消耗Na2S2O3溶液体积的平均值是25.00mL,因此消耗Na2S2O3的物质的量是0.025L×0.1mol/L=0.0025mol,根据方程式2Cu2++5I-=2CuI↓+![]() 、I
、I![]() +2
+2![]() =
=![]() +3I-可知2Cu2+~
+3I-可知2Cu2+~![]() ~2
~2![]() ,则铜离子的物质的量是0.0025mol,其浓度是
,则铜离子的物质的量是0.0025mol,其浓度是![]() =0.1250mol·L-1;
=0.1250mol·L-1;
(2)用移液管量取20.00mLCu2+的溶液时俯视刻度线,读数偏小,因此导致消耗Na2S2O3溶液体积偏小,所以最终测得的Cu2+的浓度将偏低。


科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料,下列说法中错误的是( )
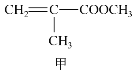
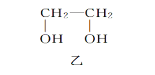
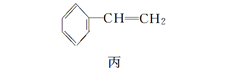
A.1mol乙可与2mol钠完全反应生成1mol氢气
B.三种物质中只有甲和丙能够使酸性高锰酸钾溶液褪色
C.甲和丙在一定条件下发生相同类型的反应
D.乙能与乙二酸反应成环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图像,其中说法正确的是

A. 由图Ⅰ知,反应在 T1、T3 处达到平衡
B. 由图Ⅰ知,该反应的△H<0
C. 由图Ⅱ知,t3时采取降低反应温度的措施
D. 由图Ⅱ知,反应在 t6时,NH3 体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究氨的还原性及检验产物的性质,按下图装置进行实验(图中夹持装置已略去)。将B处的三氧化二铬加热至红热,再鼓入空气,已知:无水氯化钙可吸收氨气和水。回答下列问题:
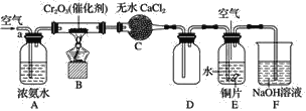
(1)B中发生反应的化学方程式是______________________________。
(2)证明氨气发生催化氧化的现象是________________,反应的方程式是________________。
(3)E中铜发生反应的离子方程式是________________________________。
(4)E中缓缓通入空气的目的是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请用化学方程式写出如何检验牙膏中存在甘油的方法___。
(2)Ca3N2是离子化合物,各原子均满足8电子稳定结构。写出Ca3N2的电子式___。
(3)常温常压下硼酸(H3BO3)晶体结构为层状,其二维平面结构如图。1mol硼酸(H3BO3)晶体中含有___mol氢键。从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大:___。
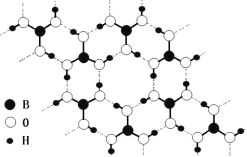
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,A是常见的金属单质、单质B是黄绿色气体、单质C是无色气体。在合适反应条件下,它们可以按下面框图进行反应;E溶液是无色溶液,F是淡绿色溶液,B和C反应发出苍白色火焰。请回答:
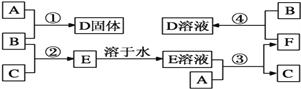
(1)A是_________,B是_________,C是_________![]() 填写化学式
填写化学式![]() ;
;
(2)反应①的化学方程式 ______________________________________;
(3)反应③的离子方程式 _____________________________________;
(4)反应④的离子方程式 ______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应 :2NaClO2 + Cl2 ===2ClO2 + 2NaCl。
下图是实验室用于制备和收集一定量较纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有CCl4液体(用于除去ClO2中的未反应的Cl2)。
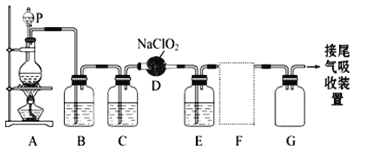
(1)仪器P的名称是_________________。
(2)写出装置A中烧瓶内发生反应的离子方程式:______________________________。
(3)B装置中所盛试剂是____________________。
(4)F为ClO2收集装置,应选用的装置是___________(填序号),其中与E装置导管相连的导管口是__________(填接口字母)。
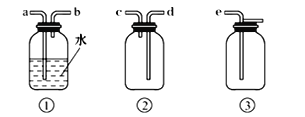
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法错误的是
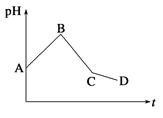
A.阳极先析出Cl2,后析出O2,阴极先产生Cu,后析出H2
B.AB段阳极只产生Cl2,阴极只产生Cu
C.BC段表示在阴极上是H+放电产生了H2
D.CD段相当于电解水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定烧碱的纯度,若烧碱中含有少量不与酸作用的可溶性杂质,试根据实验回答:
(1)准确称取4.0g烧碱样品。
(2)将样品配成250mL待测液。
(3)用____________(填仪器名称)量取25.00mL待测液于锥形瓶中,并滴加几滴甲基橙作指示剂。
(4)用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时,两眼注视____________,直到滴定终点。达到终点的具体现象是:____________。
(5)若两次实验滴定的数据如下表:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 5.00 | 28.30 |
第三次 | 25.00 | 4.00 | 24.10 |
根据上述各数据,计算烧碱的纯度:____________
(6)下列操作中,会导致所测得的烧碱的纯度偏大的是________。
a.滴定终点时,俯视刻度
b.没有用盐酸标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com