
【题目】有关物质的转化关系如下图所示(部分物质与条件已略去,其中反应②的条件是“700℃,催化剂”).G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体. 
请回答下列问题:
(1)E的化学式为 .
(2)A的电子式为 .
(3)写出反应①的离子方程式: .
(4)写出反应②的化学方程式,并标出电子转移的方向与数目: .
【答案】
(1)NO2
(2)![]()
(3)3NO2+H2O=2H++2NO3﹣+NO
(4)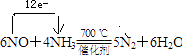
【解析】解:G是常见的红色金属单质,则G为金属Cu;D是最常见的无色液体,则D为H2O;B、H是空气的主要成分,则B、H为N2、O2;F与Cu反应生成不同气体C、E,则F应该为HNO3 , 气体E与水反应生成硝酸,则E为NO2 , C只能为NO气体;A与B反应生成H2O和NO,则A为NH3、B为O2 , 故H为N2 , 反应②的条件是“700℃,催化剂”,为NO与氨气反应生成氮气和水,(1)根据分析可知,E为二氧化氮,化学式为NO2 , 所以答案是:NO2;(2)A为氨气,氨气为共价化合物,氮原子最外层达到8电子稳定结构,氨气的电子式为 ![]() , 所以答案是:
, 所以答案是: ![]() ;(3)反应①为二氧化氮与水的反应,该反应的离子方程式为:3NO2+H2O=2H++2NO3﹣+NO,所以答案是:3NO2+H2O=2H++2NO3﹣+NO;(4)反应②为一氧化氮与氨气反应生成氮气和水,反应的化学方程式为:6NO+4NH3
;(3)反应①为二氧化氮与水的反应,该反应的离子方程式为:3NO2+H2O=2H++2NO3﹣+NO,所以答案是:3NO2+H2O=2H++2NO3﹣+NO;(4)反应②为一氧化氮与氨气反应生成氮气和水,反应的化学方程式为:6NO+4NH3 ![]() 5N2+6H2O,NO中氮元素化合价+2价变化为0价,氨气中氮元素化合价﹣3价变化为0价,电子转移总数为12e﹣ , 标出电子转移的方向与数目为:
5N2+6H2O,NO中氮元素化合价+2价变化为0价,氨气中氮元素化合价﹣3价变化为0价,电子转移总数为12e﹣ , 标出电子转移的方向与数目为: 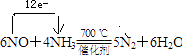 所以答案是:
所以答案是: 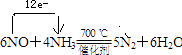 .
.


科目:高中化学 来源: 题型:
【题目】在酸性溶液中能大量共存且溶液为无色透明的离子组是( )
A. K+ 、MnO4-、Na+、Cl- B. K+、Mg2+、NO3-、Cl-
C. Na+、OH-、NH4+、CO32- D. Fe3+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节日燃放的五彩缤纷的烟花,常用一些金属化合物作为烟花的发色剂。下列金属化合物中,焰色反应呈绿色的是
A.NaClB.K2CO3C.CaCl2D.CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与 Y同族,Z 与X 形成的离子化合物的水溶液呈中性。下列说法正确的是
A. 简单离子半径:W<X<Z
B. W与X形成的化合物溶于水后溶液呈碱性
C. 气态氢化物的热稳定性:W<Y
D. 最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 
A.常压下五种元素的单质中Z单质的沸点最高
B.X和W的常见单质的分子式分别为X2和W2
C.W的氢化物沸点比X的氢化物的沸点低
D.R最高氧化物水化物的酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. Na2O2、NaClO中所含化学键类型完全相同
B. 只有活泼金属与活泼非金属元素之间才能形成离子键
C. D2O和T2O含有同种元素
D. 氯气与NaOH反应的过程中,同时又离子键、极性键和非极性键的断裂和形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体。下列说法错误的是( )
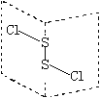
A.S2Cl2的结构中各原子均达到8电子的稳定结构
B.S2Cl2为含有极性键和非极性键的共价化合物
C.若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发新能源是解决环境污染的重要举措,其中甲醇、乙醇、甲烷都是优质的清洁燃料,可制作燃料电池。
(1)已知:①C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH1=-1366.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0kJ/mol
③H2O(g)=H2O(l) ΔH3=-44 kJ/mol。
乙醇不完全燃烧生成一氧化碳和液态水的热化学方程式为:______________________。
(2)可利用甲醇燃烧反应设计一个燃料电池。如下图1,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
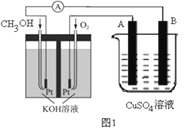
①写出燃料电池负极的电极反应式_________________。
②若利用该燃料电池提供电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是_______极(填“A”或“B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为________L。
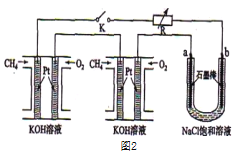
(3)某研究小组将两个甲烷燃料电池串联后如上图2作为电源,进行饱和氯化钠溶液电解实验若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量表达式为_____________(法拉第常数F=9.65×l04C/ mol),最多能产生的氯气体积为_____L(标准状况)。
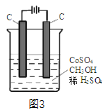
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+在阳极氧化成Co3+,生成的Co3+将甲醇氧化成CO2和H+(用石墨烯除去Co2+),现用如图3所示装置模拟上述过程,则Co2+在阳极的电极反应式为________________________除去甲醇的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW,该温度下,将浓度为amol·L-1的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A. a=b
B. 混合溶液的pH=7
C. 混合溶液中,c(H+)=![]() mol·L-1
mol·L-1
D. 混合溶液中c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com