
 ij��ѧ����С���о���������������ʱ���ı�ijһ������A2��g��+3B2��g��?2AB3��g����ѧƽ��״̬��Ӱ�죬�õ�����ͼ��ʾ�ı仯���ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ��������ݴ˿ɵó����жϽ��۲���ȷ���ǣ�������
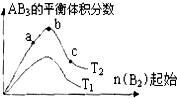
ij��ѧ����С���о���������������ʱ���ı�ijһ������A2��g��+3B2��g��?2AB3��g����ѧƽ��״̬��Ӱ�죬�õ�����ͼ��ʾ�ı仯���ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ��������ݴ˿ɵó����жϽ��۲���ȷ���ǣ�������| A���ﵽƽ��ʱA2��ת���ʴ�СΪ��c��b��a |
| B��a��b��c�����ƽ�ⳣ����ͬ |
| C���÷�Ӧһ���Ƿ��ȷ�Ӧ����T2��T1 |
| D��b��ʱ��ƽ����ϵ��A��Bԭ����֮��һ����1��1 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶ȣ�K�� | 273 | 293 | 313 | 333 | 353 | 373 |
| Ca��OH��2�ܽ�ȣ�g/100g H2O�� | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡ�����Լ��ڽྻ�ձ��У�������������ˮ����ֽ��裬���ã����ˣ�����Һ�ͳ����� | |
| ����2��ȡ������Һ���Թ��У��μ���������H2C2O4�� | ���ְ�ɫ������CaC2O4����˵�����Լ�����Ca2+���ڣ� |
| ����3��ȡ��������1�еij������Թ��У� | |
| ����4�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ܱ���Ϊδ�������������Դ����ѧ��Ԥ�⡰���ܡ�����21���������������Դ��Ŀǰ�ֽ�ˮ�������Ĺ�ҵ�Ʒ�֮һ�ǡ���-��ѭ��������Ҫ�漰���з�Ӧ��
���ܱ���Ϊδ�������������Դ����ѧ��Ԥ�⡰���ܡ�����21���������������Դ��Ŀǰ�ֽ�ˮ�������Ĺ�ҵ�Ʒ�֮һ�ǡ���-��ѭ��������Ҫ�漰���з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
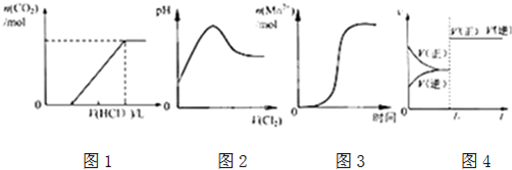
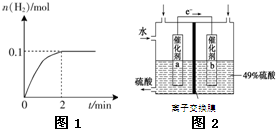
| A��ͼ1��ʾ�ں������ʵ���NaOH��Na2CO3�Ļ����Һ�еμ�0.1mol?L-1����������ʱ������������������������Ĺ�ϵ |
| B��ͼ2��ʾCl2ͨ��H2S��Һ��pH�ı仯 |
| C��ͼ3��ʾ10 mL 0.01 mol?L-1KMnO4 ������Һ�������0.1 mol?L-1 H2C2O4��Һ���ʱ��n��Mn2+�� ��ʱ��ı仯��Mn2+�Ը÷�Ӧ�д����ã� |
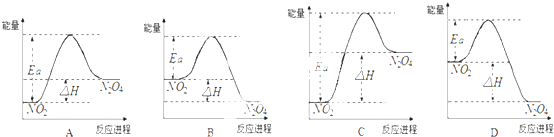
| D��ͼ4��ʾ�Ѵ�ƽ���ij��Ӧ����t0ʱ�ı�ijһ������Ӧ������ʱ��仯����ı������һ���Ǽ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ú����������Һ���������仯����ת��Ϊ���ȼ�� |
| B���ں���������������飬�ɼ�������ĸ�ʴ���� |
| C���⻯ѧ�������γ�������β���еĵ��������й� |
| D������ʹ�÷����Ͻ�֣��úϽ��۵㡢Ӳ�Ⱥ�ǿ�Ⱦ��ȴ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ����˫Ӯ�Ŀ��⣮
�о��Ϳ���CO2��CO�Ĵ��������ǻ�����������Դ����˫Ӯ�Ŀ��⣮| ʱ��t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| ��ѹǿp/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com