
| A. | 1.0mol•L-1的KNO3溶液:H+、Fe2+、SO42- | |
| B. | 酸性溶液:Na+、K+、Cl- | |
| C. | 碱性溶液:NH4+、Mg2+、Br- | |
| D. | 与铝反应产生大量氢气的溶液:Fe3+、K+、HCO3- |
分析 A.酸性条件下NO3-具有强氧化性;
B.酸性溶液下离子之间不反应;
C.可生成氢氧化镁沉淀;
D.与铝反应产生大量氢气的溶液可能呈酸性或碱性.
解答 解:A.酸性条件下NO3-具有强氧化性,Fe2+不能大量共存,故A错误;
B.酸性溶液下离子之间不反应,可大量共存,故B正确;
C.碱性条件下可生成氢氧化镁沉淀,故C错误;
D.与铝反应产生大量氢气的溶液可能呈酸性或碱性,碱性条件下Fe3+、HCO3-不能大量共存,酸性条件下HCO3-不能大量共存,故D错误.
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,注意把握常见离子的性质,题目难度不大.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 以淀粉为原料可以制取乙酸乙酯 | |
| B. | 福尔马林可用于浸制标本,是因为其能使蛋白质变性 | |
| C. | 医用酒精通常是指体积分数为75%的乙醇溶液 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液Na+、K+、MnO4-、Fe2+ | B. | 酸性溶液Fe3+、NH4+、SCN-、NH3+ | ||
| C. | 碱性溶液Na+、K+、AlO2-、SO42- | D. | 碱性溶液Ba2+、Na+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 前者生成的水少 | B. | 前者对环境的污染小 | ||
| C. | 前者燃烧产生的热量多 | D. | 前者消耗氧气量少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在氯气中燃烧制氯化钠 | |
| B. | 二氧化锰和浓盐酸共热制氯气 | |
| C. | 氯气与消石灰反应制漂白粉 | |
| D. | 氢气、氯气混合光照后的产生溶于水制盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱、小苏打、烧碱均属于碱 | B. | 盐酸、水泥合金都属于混合物 | ||
| C. | 水玻璃、玻璃、漂白粉都属于纯净物 | D. | 盐类物质一定含有金属阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 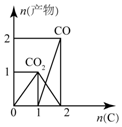 图:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 | |
| B. | 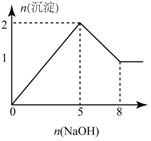 图:向含有1molMgCl2和1molAlCl3混合溶液中滴加NaOH,产生沉淀物质的量 | |
| C. | 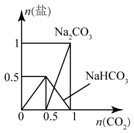 图:n(NaOH)=1mol,CO2逐步通入到NaOH溶液中反应生成的盐 | |
| D. | 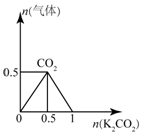 图:n(HCl)=1mol,K2CO3逐步加入到HCl溶液中,在敲口容器中生成的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲醇可以与水蒸气反应生成氢气,反应方程式如下:
甲醇可以与水蒸气反应生成氢气,反应方程式如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com