(2009?开封一模)A、B、C、D、E为原子序数依次增大的五种短周期元素,已知A的一种核素的质量数为另一种核素质量数的2倍,A和C、B和E分别位于同一主族,且B、E的质子数之和是A、C质子数之和的2倍,C、D、E这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水.试回答:
(1)写出下列元素的符号:A
H
H
、E
S
S
.
(2)C、D、E三种元素离子半径由大到小的顺序是
S 2->Na+>Al 3+
S 2->Na+>Al 3+
(填相应的离子符号).
(3)由A、B两元素形成的原子个数比为1:1化合物的电子式是
.
(4)C、D元素的最高价氧化物的水化物之间反应的离子方程式是:
Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
.
(5)用多孔石墨电极电解滴有酚酞的C元素和氯元素形成的化合物的饱和溶液,接通电源一段时间后,
阴
阴
极(填电极名称)附近出现红色,另一极的电极反应式为
2Cl--2e-═Cl2↑
2Cl--2e-═Cl2↑
,可用
湿润的碘化钾淀粉试纸
湿润的碘化钾淀粉试纸
检验该电极所得产物.

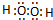
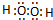
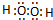 ,
,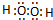 ;
;

 百年学典课时学练测系列答案
百年学典课时学练测系列答案