
(8分)为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验).
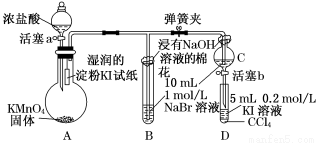
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是_________________.
(2)验证氯气的氧化性强于碘的实验现象是________________.
(3)B中溶液发生反应的离子方程式是__________________________.
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是____ ____.
(5)过程Ⅲ实验的目的是___ _ __.
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下________,得电子能力逐渐减弱.
科目:高中化学 来源:2015-2016学年黑龙江铁人中学高一上第一阶段测化学卷(解析版) 题型:选择题
将质量分数为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是
A.c2=c1 B.c2<2c1 C.c2>2c1 D.c2=2c1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
在其他条件不变时,某气体的体积与温度(K)成正比。在不同温度时有的气体还会形成不同分子数的缔合物。一下是该气态物质在不同温度时测得的密度。
温度/K | 200 | 400 | 800 | 1600 |
密度/g·cm-3 | 3.21 | 0.81 | 0.20 | 0.11 |
今测得1600K时该物质的分子组成为AB2,则在其余温度时它的化学式应分别为(800K)时:___________,(400K)时: ,(200K)时: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
在标准状况下,对下列对这四种气体的关系从大到小表达正确的是
①6.72 L CH4 ②3.01×1023个HCl分子 ③13.6 g H2S ④0.2 mol NH3
a.体积:②>③>①>④ b.密度:②>③>④>①
c.质量:②>③>①>④ d.氢原子个数:①>③>④>②
A.abc B.bcd C.abcd D.acd
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
下列选项中的诗旬内容基本不涉及化学变化的是
A.王安石的《元日》 :“爆竹声中一岁除,春风送暖入屠苏”
B.刘禹锡的《浪淘沙》 :“美人首饰侯王印,尽是江中浪底来”
C.刘琨的《重赠卢谌》 :“ 何意百炼钢,化为绕指柔”
D.李商隐的《无题》 :“春蚕到死丝方尽,蜡炬成灰泪始干”
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省龙东南四校高一下学期期末联考化学试卷(解析版) 题型:选择题
已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ,某有机物分解的反应可表示为:

若在反应中消耗了1 mol乙烷(反应物),则有关该反应的说法正确的是
A.该反应放出251.2 kJ的热量 B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量 D.该反应吸收125.6 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省龙东南四校高一下学期期末联考化学试卷(解析版) 题型:选择题
下列各组顺序的排列不正确的是
A.酸性强弱:HClO4>H2SO4>H3PO4 B.离子半径:Na+>Mg2+>Al3+>F-
C.热稳定性:HCl>H2S>PH3>SiH4 D.氧化性:K+ < Na+ < Mg2+ < Al3+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北荆州中学高二上期中测试化学试卷(解析版) 题型:填空题
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)  CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n(H2O)/ mol |
0 | 1.20 | 0.60 |
t1 | 0.20 | |
t2 | 0.80 |
依据题意回答下列问题:
(1)反应在t1min内的平均速率为v(H2)= mol·L-1·min-1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)= mol。
(3)温度升至800℃,上述反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”)。
(4)700℃时,向容积为2L的密闭容器中充入CO(g)、H2O(g) 、CO2(g)、H2(g)的物质的量分别为1.20mol、2.00mol、1.20mol、1.20mol,则此时该反应v(正) v(逆)(填“>”、“<”或“=”)。
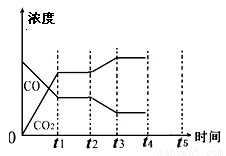
(5)该反应在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是 、 (写出两种)。
(6)若该容器绝热体积不变,不能判断反应达到平衡的是 。
①体系的压强不再发生变化
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化
⑥v(CO2)正=v(H2O)逆
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南湘潭、岳阳一中高一上联考化学试卷(解析版) 题型:选择题
关于容量瓶的叙述:①是配制准确物质的量浓度溶液的仪器;②不宜长时间贮存溶液;③能用来加热;④使用之前要检查是否漏水。这些叙述中正确的有
A.①②③④
B.②③
C.①②④
D.②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com