
【题目】近段时间,雾霾笼罩中原大地,长江南北,其中雾属于下列分散系中的
A.溶液 B.悬浊液 C.乳浊液 D.胶体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A.Na2O2是淡黄色固体, Na2O 是白色固体, 二者都能与水反应生成 NaOH
B.钠质地柔软,可用小刀切割,保存在煤油中
C.钠的还原性很强,只能以化合态存在于自然界
D.Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成 O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2与SO2能发生反应:NO2+SO2![]() SO3+NO,某研究小组对此进行相关实验探究。
SO3+NO,某研究小组对此进行相关实验探究。
(1)已知:2NO(g)+O2(g) ![]() 2NO2(g) △H=-113.0 kJ mol-1
2NO2(g) △H=-113.0 kJ mol-1
2SO2(g)+O2(g) ![]() 2SO3(g) △H=-196. 6 kJ mol-1
2SO3(g) △H=-196. 6 kJ mol-1
则NO2(g)+SO2(g) ![]() SO3(g)+N0(g) △H= ________.
SO3(g)+N0(g) △H= ________.
(2)实验中,尾气可以用碱溶液吸收。NaOH溶液吸收N02时,发生的反应为:
2NO2+2OH- =NO2- +NO3- +H2O,反应中形成的化学键是________(填化学键的类型);用NaOH溶液吸收少量SO2的离子方程式为____________。
(3)在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。 部分实验结果如图所示:
①当容器内_______(填标号)不再随时间的变化而改变时,可以不断反应达到了化学平衡状态。
a.气体的压强
b.气体的平均摩尔质量
c.气体的密度
d.NO2的体积分数
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是________。

③若A点对应实验中,S02(g)的起始浓度为c0 molL-1 ,经过t min达到平衡状态,该时段化学反应速率![]() (N02)= _________molL-1min -1.
(N02)= _________molL-1min -1.
④图中C、D两点对应的实验温度分别为Tc和Td,通过计算判断::Tc_____Td(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、X、Y、Z、Q、R、T分别代表原子序数依次增大的短周期元素。元素A是原子半径最小的元素;X、Y、Z同周期且相邻,都是蛋白质的组成元素;X、R同族,Q与T原子的最外层电子数之和是R原子最外层电子数的2倍,T单质为淡黄色固体。U是d区元素,U2+的核外最高能级有2对成对电子。请回答下列问题:
(1)Y元素在周期表中的位置____________,位于周期表_____区;Q原子的核外电子排布式为________。
(2)X、Y、Z元素的第一电离能由大到小的顺序是________________。
(3)TZ3分子为________分子(填“极性”或“非极性”),YZ2-离子的VSEPR模型名称是________。(每空2分)
(4)Z和T的简单气态氢化物稳定性好的是_______(填化学式),原因是________________________________________________________________。
(5)A、X、Z、可形成分子式为A2XZ的有机物,则该化合物分子中B原子的轨道杂化类型是________;1mol该分子中含有π键的数目是________。
(6)通常情况下,U2+的溶液很稳定,它与YH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为配位数不变的+3价配离子.该反应的离子方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,在生产、生活中用途广泛。
(1)已知:
共价键 | 键能/ kJ·mol-1 |
H―H | 436 |
N≡N | 946 |
N―H | 391 |
注:拆开气态物质中1 mol某种共价键需要吸收的能量,就是该共价键的键能。
N2 (g)+3 H2 (g)![]() 2 NH3 (g) H =____kJ·mol-1
2 NH3 (g) H =____kJ·mol-1
(2)一定温度下,向恒容的密闭容器中充入N2和H2发生反应:N2 +3H2 ![]() 2NH3,测得各组分浓度随时间变化如图1所示。
2NH3,测得各组分浓度随时间变化如图1所示。

①表示c(N2)的曲线是__(填“曲线A”、“曲线B”或“曲线C”)。
②0~t0时用H2表示反应速率v(H2)____mol·L-1·min-1。
③下列能说明该反应达到平衡的是____。
a.混合气体的压强不再变化
b.2c(H2)= 3c(NH3)
c.混合气体的质量不再变化
d.NH3的体积分数不再变化
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图2所示:

①电极b名称是____。
②电解质溶液中OH-离子向____移动(填“电极a”或“电极b”)。
③电极a的电极反应式为____。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物。
(1)Cr3+的核外电子排布式为____________________, 配离子[Cr(H2O)6] 3+中,与Cr3+形成配位键的原子是________(填元素符号)。
(2)NH3是一种很好的配体,氨分子是____________(填“极性”或“非极性”)分子,NH3的沸点_____________(填“高于”、“等于”或“低于”)AsH3。
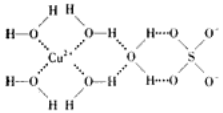
(3)科学家通过X-射线测得胆矾(CuSO4·5H2O)的结构示意图可简单表示如下:
图中虚线表示的作用力为_______________________;
(4)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,呈正四面体结构的原子团是_________,其中心原子的杂化类型是______。
(5)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于_________(填标号)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2-丁烯有顺、反两种异构体,在某条件下两种气体处于平衡,下列说法正确的是 ( )
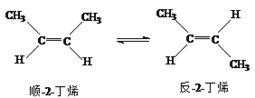 △H= -4.2 kJ/mol
△H= -4.2 kJ/mol
A. 反-2-丁烯和顺-2-丁烯具有相同的熔沸点。
B. 顺-2-丁烯比反-2-丁烯更稳定。
C. 加压和降温有利于平衡向生成顺-2-丁烯反应方向移动
D. 反-2-丁烯和顺-2-丁烯的核磁共振氢谱都有两个峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置收集气体并验证其某些化学性质,正确的是

选项 | 气体 | 试剂② | 现象 | 结论 |
A | NH3 | 酚酞试液 | 溶液变红色 | NH3的水溶液显碱性 |
B | Cl2 | 紫色石蕊试液 | 溶液立即褪色 | Cl2有氧化性 |
C | SO2 | 溴水 | 溶液褪色 | SO2有漂白性 |
D | X(能形成酸雨) | KI淀粉溶液 | 溶液变蓝 | X是NO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com