
【题目】下列关于有机物的说法中,正确的一组是
![]() 纤维素、油脂、蛋白质一定条件下在人体内都能发生水解反应
纤维素、油脂、蛋白质一定条件下在人体内都能发生水解反应
![]() “乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
![]() 除去乙酸乙酯中残留的乙酸,可加过量饱和
除去乙酸乙酯中残留的乙酸,可加过量饱和![]() 溶液振荡后,静置分液
溶液振荡后,静置分液
![]() 石油的裂化、煤的干馏、煤的液化都是化学变化
石油的裂化、煤的干馏、煤的液化都是化学变化
![]() 淀粉遇碘酒变蓝色,葡萄糖能与新制
淀粉遇碘酒变蓝色,葡萄糖能与新制![]() 悬浊液发生反应.
悬浊液发生反应.
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组利用芳香族化合物A制取有机物F的合成路线如下:

回答下列问题:
(1)A的分子式为____________,B→C的反应类型为________。
(2)足量的D与Na2CO3溶液发生反应的化学方程式:__________。
(3)E的结构简式为___________________________。
(4)碳原子上连有4个不同的原子或基团时,该碳原子称为手性碳。写出上述合成路线中含有手性碳的物质结构简式并用星号( * )标出手性碳:__________________________。
(5)芳香族化合物M与A互为同分异构体,且M能发生银镜反应.则M的结构有_____种(不考虑立体异构);其中核磁共振氢谱显示有4种不同化学环境的氢且峰面积之比为6: 2: 1 : 1的结构简式有________(任写-种)。
(6)结合已知信息写出用1-溴丙烷和苯为原料制备![]() 的合成路线(其他试剂任选)。_______________。
的合成路线(其他试剂任选)。_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五种元素,其中
五种元素,其中![]() 、
、![]() 、
、![]() 属于同一周期,
属于同一周期,![]() 原子最外层的
原子最外层的![]() 能级电子数等于次外层的电子总数,
能级电子数等于次外层的电子总数,![]() 原子最外层中有2个未成对电子。已知
原子最外层中有2个未成对电子。已知![]() 、
、![]() 、
、![]() 原子核内的质子数均与中子数相等,且
原子核内的质子数均与中子数相等,且![]() 元素可分别与
元素可分别与![]() 、
、![]() 、
、![]() 、
、![]() 生成
生成![]() 型化合物,在
型化合物,在![]() 中,
中,![]() 与
与![]() 的质量比为
的质量比为![]() ,在
,在![]() 中,
中,![]() 与
与![]() 的质量比为
的质量比为![]() 。请回答下列问题:
。请回答下列问题:
(1)写出![]() 、
、![]() 两种元素的元素符号:
两种元素的元素符号:![]() ______,
______,![]() ______。
______。
(2)写出![]() 元素原子的电子排布式:______。
元素原子的电子排布式:______。
(3)指出![]() 在元素周期表中的位置:______。
在元素周期表中的位置:______。
(4)比较![]() 、
、![]() 、
、![]() 三种元素的第一电离能的大小:______(填元素符号,下同)。
三种元素的第一电离能的大小:______(填元素符号,下同)。
(5)比较![]() 元素和
元素和![]() 元素的电负性的相对大小:______。
元素的电负性的相对大小:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒压下,在一个容积可变的容器中发生如下反应:A(g)+B(g)C(g)
(1)若开始时放入1 mol A和1 mol B,达到平衡后,生成amol C,这时A的物质的量为__mol。
(2)若开始时放入3 mol A和3 mol B,达到平衡后,生成C的物质的量为__mol
(3)若开始时放入xmol A、2 mol B和1 mol C,达到平衡后,A和C的物质的量分别为ymol和3amol,则x=__,y=__。平衡时,B的物质的量__(填编号)。
A.大于2 mol B.等于2 mol C.小于2 mol D.可能大于、等于或小于2 mol
(4)若在(3)的平衡混合物中再加入3 mol C,待再次达到平衡后,C的物质的量分数是__。
(5)若维持温度不变,在一个与反应前起始体积相同,且容积固定的容器中发生上述反应。开始时放入1 mol A和1 mol B到达平衡后生成bmol C。将b与(1)小题中的a进行比较__(填编号)。作出此判断的理由是__。
A.a>b B.a<b C.a=b D.不能比较a和b的大小。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图可设计成多种用途的电化学装置。下列分析正确的是
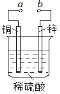
A.当a和b用导线连接时,溶液中的SO42-向铜片附近移动
B.当a和b用导线连接时,铜片上发生的反应为:2H++2e →H2↑
C.将a与电源正极相连可以保护锌片,叫牺牲阳极的阴极保护法
D.a和b用导线连接后,电路中通过0.02 mol电子时,产生0.02 mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是锂、氦、汞原子的吸收光谱和发射光谱。其中图______是原子由基态转化为激发态时的光谱,图______是原子由激发态转化为基态时的光谱。不同元素的原子光谱上的特征谱线不同,请在图中将同种元素原子的吸收光谱和发射光谱连接起来______。
①![]() ②
②![]()
③![]() ④
④![]()
⑤![]() ⑥
⑥![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中,可逆反应:H2(g) + I2(g) ![]() 2HI (g)达到平衡的标志是( )
2HI (g)达到平衡的标志是( )
①H2、I2、HI的分子数之比为1∶1∶2
②混合气体的密度保持不变
③单位时间形成n mol H—H键,同时形成2n mol H—I键
④混合气体的颜色不再发生变化
⑤混合气体的平均相对分子质量不再发生变化
⑥容器压强不再发生变化
⑦H2的体积分数不再发生变化
A.①②④⑤B.③④C.③④⑦D.②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在我们的日常生活中,电化学技术与我们密切相关。根据所学电化学知识,回答下列问题:
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_____________。
A.CH4(g)+O2(g)=CO2(g)+H2O(g) △H<0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(l) △H<0
C.2H2O(l)=2H2(g)+O2(g) △H>0
(2)以熔融KCO3为电解质溶液,依据所选反应设计一个原电池,其负极反应式为______________________________。
(3)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与下图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:

①若X和Y均为惰性电极,a为MgCl2溶液,则电解时的化学反应方程式为______________________________。
②若X和Y为惰性电极,a为CuSO4溶液,通电一段时间后,向所得溶液中加入0.2mol Cu(OH)2粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为_________________。
③若X、Y分别为铁和铜,a为H2SO4溶液,则电解池的总反应式为___________________________。
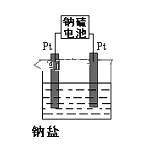
(4)现有有一种新型的高能电池——钠硫电池(熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质),反应式为:2Na+xS![]() Na2Sx,上述电解都是用该电池作电源(如图)该电池的正极反应为______________________。
Na2Sx,上述电解都是用该电池作电源(如图)该电池的正极反应为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述正确的是( )
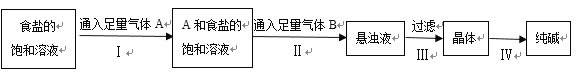
A.第Ⅱ步的离子方程式为Na++NH3+H2O+CO2→NaHCO3↓+NH4+
B.第Ⅲ步得到的晶体是Na2CO310H2O
C.A气体是CO2,B气体是NH3
D.第Ⅳ步操作的过程主要有溶解、蒸发、结晶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com