
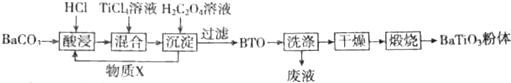
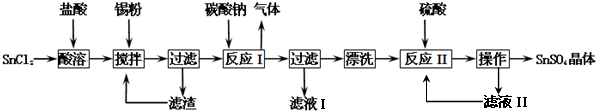
���� ̼�ᱵ�����ᷴӦ�����Ȼ�����Ȼ���Ȼ��������Ȼ�̼�����ᷴӦ����BaTiO��C2O4��2•4H2O��ͬʱ�õ�ΪHCl��HCl��ѭ�����ã��������ˡ�ϴ�ӡ�������յõ�BaTiO3��
��1�������������ĽӴ����������߷�Ӧ���ʣ�����XΪHCl��
��2��FeTiO3�뽹̿��������Ӧ�õ�CO��TiCl4����������ǿ�����ԣ��������Ȼ�����TiCl4��ˮ��Һ�з���ˮ�⣻
��3��BTO����ḽ��HCl�ȣ��������ữ����������Һ�������һ��ϴ��Һ���Ƿ��������ӽ����жϣ�
BaTiO��C2O4��2•4H2O���գ������ֽⷴӦ����BaTiO3���������ֽ�ΪCO��CO2������H2O��g�����ɣ�
��� �⣺̼�ᱵ�����ᷴӦ�����Ȼ�����Ȼ���Ȼ��������Ȼ�̼�����ᷴӦ����BaTiO��C2O4��2•4H2O��ͬʱ�õ�ΪHCl��HCl��ѭ�����ã��������ˡ�ϴ�ӡ�������յõ�BaTiO3��
��1�������������ĽӴ����������߷�Ӧ���ʣ�����XΪHCl��
�ʴ�Ϊ����߷�Ӧ���ʣ�HCl��
��2��FeTiO3�뽹̿��������Ӧ�õ�CO��TiCl4����������ǿ�����ԣ��������Ȼ�������Ӧ����ʽΪ��2FeTiO3+6C+7Cl2$\frac{\underline{\;900��\;}}{\;}$6CO+2TiCl4+2FeCl3����TiCl4��Һʱ��ͨ���ǽ�TiCl4����Ũ���ᣬȻ���ټ�ˮϡ�ͣ���Ŀ���ǣ�����Ti4+ˮ�⣬
�ʴ�Ϊ��2FeTiO3+6C+7Cl2$\frac{\underline{\;900��\;}}{\;}$6CO+2TiCl4+2FeCl3������Ti4+ˮ�⣻
��3��BTO����ḽ��HCl�ȣ�BTO������ˮ���ϴ�Ӻ��ж�����ϴ�Ӹɾ���ʵ������������ǣ�ȡ���һ��ϴ��Һ���Ƚ������ᣬ�ٽ�����������Һ��û�а�ɫ�������ɣ�˵��ϴ�Ӹɾ���
BaTiO��C2O4��2•4H2O���գ������ֽⷴӦ����BaTiO3���������ֽ�ΪCO��CO2������H2O��g�����ɣ���Ӧ����ʽΪ��BaTiO��C2O4��2•4H2O$\frac{\underline{\;\;��\;\;}}{\;}$BaTiO3+2CO��+2CO2��+4H2O��
�ʴ�Ϊ��ȡ���һ��ϴ��Һ���Ƚ������ᣬ�ٽ�����������Һ��û�а�ɫ�������ɣ�˵��ϴ�Ӹɾ���BaTiO��C2O4��2•4H2O$\frac{\underline{\;\;��\;\;}}{\;}$BaTiO3+2CO��+2CO2��+4H2O��
���� ���⿼�������Ʊ��������̣��漰�Բ����ķ������ۡ����Ӽ��顢����Ϣ��ȡ��Ӧ�õȣ����ضԻ�ѧ����Ŀ��飬��������Ԫ�ػ�����֪ʶ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O | B�� | CaCl2 | C�� | NH4Cl | D�� | HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
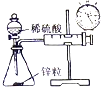 |  |  | 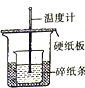 |
| A������п��ϡ���ᷴӦ������ | B��֤���ǽ����ԣ�Cl��C��Si | C����������к͵ζ�ʵ�� | D���ⶨ�к��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
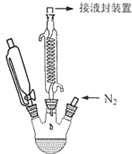 ��ï���Ļ�ѧʽΪ��C5H5��2Fe������һ�ֳȻ�ɫ��״���壬�۵�173--174�棬100�����������������е�249�棬������ˮ�������ڼ״����Ҵ������Ѻͱ����л��ܼ������������ܵĻ��ȼ�����Ӽ���ʵ�����Ʊ���ï���ķ�Ӧԭ��Ϊ��8KOH+2C5H6+FeCl2•4H2O$\frac{\underline{\;\;��\;\;}}{\;}$��C5H5��2Fe+2KCl+6KOH•H2Oʵ��װ����ͼ��ʾ�����ȼ���������װ��δ��������
��ï���Ļ�ѧʽΪ��C5H5��2Fe������һ�ֳȻ�ɫ��״���壬�۵�173--174�棬100�����������������е�249�棬������ˮ�������ڼ״����Ҵ������Ѻͱ����л��ܼ������������ܵĻ��ȼ�����Ӽ���ʵ�����Ʊ���ï���ķ�Ӧԭ��Ϊ��8KOH+2C5H6+FeCl2•4H2O$\frac{\underline{\;\;��\;\;}}{\;}$��C5H5��2Fe+2KCl+6KOH•H2Oʵ��װ����ͼ��ʾ�����ȼ���������װ��δ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
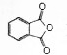 ����һ�������¿��Ƶ÷�̪������ӽṹ��ͼ��ʾ
����һ�������¿��Ƶ÷�̪������ӽṹ��ͼ��ʾ ������˵����ȷ���ǣ�������
������˵����ȷ���ǣ�������| A�� | �����Ʒ�̪�ķ�Ӧ����ȡ����Ӧ | |
| B�� | ��̪�����е�̼ԭ���п��ܹ�����ͬһƽ�� | |
| C�� | ����̪���ھƾ���ɵķ�̪�Լ����������Ի�����ˮ��Һ�п��ܻ���ְ�ɫ���� | |
| D�� | ����NaOH��Һ��Ӧ��1mol��̪��������4molNaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
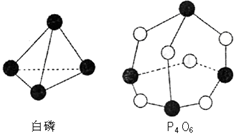 ��ѧ��Ӧ����Ϊ�ɽ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�������������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ•mol-1��P-P��198��P-O��360��O-O��498����ӦP4�����ף�+3O2=P4O6�ķ�Ӧ�ȡ�HΪ��������
��ѧ��Ӧ����Ϊ�ɽ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�������������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ•mol-1��P-P��198��P-O��360��O-O��498����ӦP4�����ף�+3O2=P4O6�ķ�Ӧ�ȡ�HΪ��������| A�� | -1638kJ/mol | B�� | +1638kJ/mol | C�� | -126kJ/mol | D�� | +126kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com