
 |  |  | 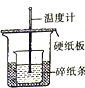 |
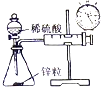
| A.测量锌与稀硫酸反应的速率 | B.证明非金属性:Cl、C、Si | C.进行酸碱中和滴定实验 | D.测定中和热 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.通过测定一定时间内收集气体多少测量锌与稀硫酸反应速率;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
D.碱液只能盛放在碱式滴定管中;
D.中和热测定中需要用环形玻璃棒搅拌混合液.
解答 解:A.通过测定一定时间内收集气体多少测量锌与稀硫酸反应速率,需要秒表、针筒等仪器,故A正确;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,HCl不是Cl元素的最高价氧化物的水化物,且盐酸具有挥发性,生成的二氧化碳中含有HCl,干扰二氧化碳的检验,该实验不能判断非金属性强弱,故B错误;
D.碱液只能盛放在碱式滴定管中,NaOH能和玻璃中二氧化硅反应生成粘性物质硅酸钠导致活塞打不开,故C错误;
D.中和热测定中需要用环形玻璃棒搅拌混合液,否则混合溶液温度不均匀,导致测定不准确,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及反应速率测定、非金属性强弱判断、仪器的使用、中和热的测定等知识点,明确实验原理及实验基本操作是解本题关键,易错选项是B,知道非金属强弱判断方法,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸保存在棕色带橡胶塞的试剂瓶中 | |
| B. | 漂粉精露置在空气中 | |
| C. | 烧碱溶液可保存在带玻璃塞试剂瓶中 | |
| D. | 可用铝制容器存放浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该现象说明了NaHCO3难溶于水 | |
| B. | 滤液中的c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 滤液中c(Na+)+c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| D. | 滤液中c(Cl-)>c(NH4+)>c(HCO3-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的H2O与CH2D2含有的质子数相同 | |
| B. | 室温下CH3COONH4溶液pH=7,1L 0.1mol•L-1该溶液中NH4+离子数为0.1NA | |
| C. | 标准状况下,6.72 L NO2与水充分反应转移的电子数为0.2NA | |
| D. | 1mol CH3COOC2H5在足量NaOH溶液中水解得到乙醇分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用萃取法分离汽油和水的混合液 | |
| B. | 用结晶法提纯NaC1和KNO3混合物中的KN03 | |
| C. | 直接蒸馏酒精溶液得到无水乙醇 | |
| D. | 除去FeC13溶液中少量的FeC12,加入足量的铁屑,充分反应后,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\overline{v}$(NH3)=0.01 mol/(L•s) | B. | $\overline{v}$(O2)=0.00l0 mol/(L•s) | ||
| C. | $\overline{v}$(NO)=0.00l0 mol/(L•s) | D. | $\overline{v}$(H2O)=0.045 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4 和C3H6的混合物的质量为a g,所含碳氢键数目为$\frac{a{N}_{A}}{7}$ | |
| B. | 标准状况下,2.24 L 2H35Cl 中所含中子数为1.8NA | |
| C. | 50 mL 12 mol•L-1 盐酸与足量MnO2 共热,转移的电子数为0.3NA | |
| D. | 1 L O.lmol•L-1的NaHCO3 溶液中HCO3-和CO32-的离子数之和为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
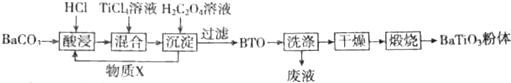
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1molNa2O2和22.4LCO2反应,转移电子数为1mol | |
| B. | 将钠投入到CuSO4溶液中,可以置换生成Cu | |
| C. | 将Na2O2投入到FeSO4溶液中,可生成红褐色沉淀 | |
| D. | 常温下铜与稀硫酸不反应,加入KNO3晶体后,可生成气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com