
| A、石灰水与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | ||||
B、NH4HSO4溶液与足量的NaOH溶液混合加热:NH4++HSO4-+2OH-
| ||||
| C、二氧化硫通入氯化铁溶液:SO2+Fe3++2H2O═SO42-+Fe2++4H+ | ||||
| D、AgNO3溶液中加入过量的氨水:Ag++NH3?H2O═AgOH↓+NH4+ |
| ||


科目:高中化学 来源: 题型:
| A、该电池的正极为锌 |
| B、电池正极反应式为:2MnO2+2e-+2H2O═2MnO (OH)+2OH- |
| C、当 0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023 |
| D、该电池反应中二氧化锰起催化剂作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
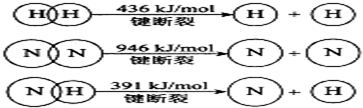
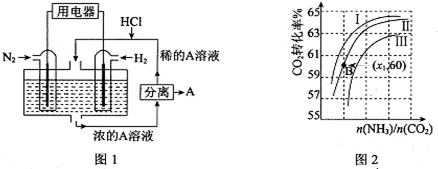
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
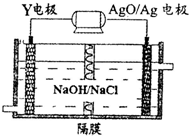 短周期元素X、Y、Z、W原子序数依次增大.X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中.请回答:
短周期元素X、Y、Z、W原子序数依次增大.X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
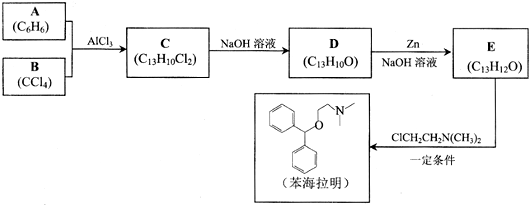
 +CH3Cl
+CH3Cl| AlCl3 |
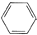 -CH3+HCl
-CH3+HCl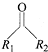
| Zn |
| NaOH溶液 |
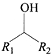 (1R、R2代表羟基)
(1R、R2代表羟基)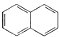 结构;②能与FeCl3溶液发生显色反应,共有
结构;②能与FeCl3溶液发生显色反应,共有查看答案和解析>>
科目:高中化学 来源: 题型:
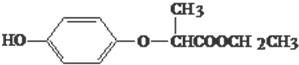
| A、HPE不能跟浓溴水反应 |
| B、1molHPE最多可以和2mol NaOH反应 |
| C、HPE在核磁共振氢谱中有6个峰 |
| D、HPE分子中有2个手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
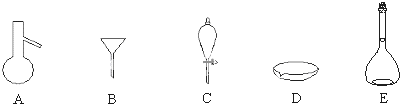
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com