
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示。有关说法不正确的是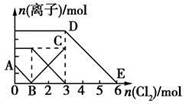
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中n(FeBr2)=3 mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+):n(I-):n(Br-)=3:1:2 |
科目:高中化学 来源: 题型:单选题
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS或PbS,慢慢转化为铜蓝(CuS)。下列分析正确的是
| A.CuS的溶解度大于PbS的溶解度,Ksp(ZnS)<Ksp(CuS) |
| B.原生铜的硫化物具有还原性,而铜蓝没有还原性 |
| C.CuSO4与ZnS反应的离子方程式是Cu2++S2-=CuS↓ |
| D.整个过程涉及的反应类型有氧化还原反应和复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是
| A.F2、K、HCl | B.Cl2、Al、H2 |
| C.SO2、Na、Br2 | D.O2、SO2、H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3﹑H2O﹑Cl2、H+ 、Cl-和Co2+。下列叙述不正确的是
| A.氧化产物为Cl2 |
| B.氧化剂与还原剂的物质的量之比为1∶2 |
| C.若有3mol H2O生成,则反应中有2mol电子转移 |
| D.当该反应生成2.24L Cl2时,则反应中有0.1mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应或过程一定不是氧化还原反应的是( )
| A.ΔH<0 的反应 | B.古人用热分解法制水银 |
| C.用明矾净水 | D.实验室用浓盐酸和MnO2制Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
19.2g铜与适量的浓HNO3反应,铜全部反应后,共收集到11.2 LNO和NO2混合气体(标准状况),反应消耗HNO3的物质的量是( )
| A.0.8 mol | B.1.1 mol | C.1.2 mol | D.2.0 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中能肯定A金属比B金属金属性强的是 ( )
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A原子的电子层数比B原子的电子层数多 |
| C.1mol A从酸中置换H+生成的H2比1mol B从酸中置换H+生成的H2多 |
| D.常温时,A能从水中置换出氢,而B不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| B.能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
1.52 g铜镁合金完全溶解于50 mL密度为1.40 g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2∶1 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol·L-1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com