

| ѹǿ/Mpa/�������/%/�� | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 82.0 |
| [H2CO3][OH-] |
| [HCO3-] |
| Kw |
| Ka(H2CO3) |
| 10-14 |
| 4��10-7 |
| 2ax |
| a-ax+2ax |
| [H2CO3][OH-] |
| [HCO3-] |
| Kw |
| Ka(H2CO3) |
| 10-14 |
| 4��10-7 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������������ʵ���Ũ�ȵ�NaCl��aq��������������NaClO��aq������������ |
| B��pH=3��������Һ��ˮ�ĵ���̶ȵ���pH=11�İ�ˮ��Һ��ˮ�ĵ���̶� |
| C��0.1 mol/L��NaHA��ҺpH=5������Һ��c��HA-����c��H+����c��A2-����c��H2A�� |
| D����NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ����û��Һ��c��Na+����c��NH4+����c��SO42-����c��OH-��=c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
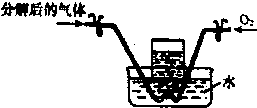 ��֪Fe��NO3��2���ȷֽ����Ϊ���������NO2��O2��ij��ȤС��ͬѧ�Թ��������Fe�Ļ��������������̽����
��֪Fe��NO3��2���ȷֽ����Ϊ���������NO2��O2��ij��ȤС��ͬѧ�Թ��������Fe�Ļ��������������̽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������������������ܣ��ٽ���������Դ�ķ�չ |
| B�����ú��ܡ�ˮ�⡢��ϫ�ȷ��磬���Լ��ٻ��������ú�Ȼ�ʯȼ�ϵ�ʹ�� |
| C��H2���������ɫ��Դ�����õ��ˮ�ķ������л�� |
| D���ƹ�����̫���ܡ����ܵ�����ϵͳ��������ʵ�ֳ��еġ����칤�̡� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com