
【题目】研究电解质在水溶液中的平衡能了解它的存在形式。
(1)已知部分弱酸的电离常数如下表:
化学式 | HF | H2CO3 | H2S |
电离平衡常数K(25℃) |
|
|
|
①写出H2S的Ka1的表达式:________________。
②常温下,pH相同的三种溶液NaF、Na2CO3、Na2S,物质的量浓度最小的是_______。
③将过量H2S通入Na2CO3溶液,反应的离子方程式是_______________。
(2)室温下,用0.100 mol·L-1 盐酸溶液滴定20.00 mL 0.100 mol·L-1 的氨水溶液,滴定曲线如图所示。(忽略溶液体积的变化,①②填“>”“<”或“=”)
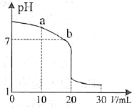
①a点所示的溶液中c(NH3·H2O)___________c(Cl-)。
②b点所示的溶液中c(Cl-)___________c(NH4+)。
③室温下pH=11的氨水与pH=5的NH4Cl溶液中,由水电离出的c(H+)之比为__________。
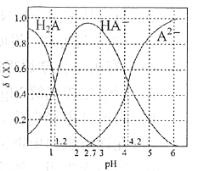
(3)二元弱酸H2A溶液中H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示。则H2A第二级电离平衡常数Ka2=___________。
【答案】c(H+)·c(HS-)/c(H2S) Na2S H2S+CO32-=HCO3-+HS < = 1:106 10-4.2
【解析】
Ka为弱酸的电离平衡常数,Ka值越大,在相同条件下,酸性越强,即酸性有HF>H2CO3>H2S>HCO3->HS-,多元弱酸电离分步,以第一步为主,同理,多元弱酸盐水解也分步,以第一步为主,据此解答。
(1)①平衡常数为生成物浓度的幂之积与反应物浓度幂之积的比值,根据H2SO3![]() HSO3- +H+可知Ka的表达式为c(H+)·c(HS-)/c(H2S);
HSO3- +H+可知Ka的表达式为c(H+)·c(HS-)/c(H2S);
②相同浓度的NaF、Na2CO3、Na2S中,由于酸性HF>HCO3->HS-,根据越弱越水解,S2-水解程度最大,产生的OH-浓度最大,pH值最大;故pH相同的三种溶液NaF、Na2CO3、Na2S,浓度最小的为Na2S,答案为:Na2S;
③将过量H2S通入Na2CO3溶液,根据强酸制弱酸的原理,由于酸性H2CO3>H2S>HCO3->HS-,所以,即便H2S过量,也只能生成HCO3-和HS-,而不能生成CO2,答案为:H2S+ CO32-=HCO3-+HS-;
(1)①用0.100 mol·L-1 盐酸溶液滴定20.00 mL 0.100 mol·L-1 的氨水溶液时,在a点消耗盐酸10.00 mL时,反应后生成的氯化铵和剩余的NH3·H2O的物质的量相等,若只考虑氯化铵电离,c(NH4+)和c(Cl-)相等,但NH4+要水解消耗,a点pH大于7,呈碱性,以电离为主,产生的NH4+多,所以c(Cl-)<c(NH4+);
②b点溶液中存在电荷守恒,c(NH4+)+ c(H+) =c(Cl-) +c(OH-),b点pH值为7,c(H+) = c(OH-),故c(NH4+) =c(Cl-),答案为:=;
③pH=11的氨水,氨水不能电离出H+,溶液中H+就是水电离出的H+,c(H+)为1×10-11, pH=5的NH4Cl溶液中铵根水解,溶液显酸性,溶液中水电离出的c(H+)为1×10-5,故由水电离出的c(H+)之比为1:106;
(3)H2A的二级电离为HA-![]() H++A2-,Ka2=c(H+)×c(A2-)/c(HA-),电离平衡常数是温度的常数,从图中取c(A2-)=c(HA-)特殊点,Ka2= c(H+)=10-4.2,故答案为:10-4.2。
H++A2-,Ka2=c(H+)×c(A2-)/c(HA-),电离平衡常数是温度的常数,从图中取c(A2-)=c(HA-)特殊点,Ka2= c(H+)=10-4.2,故答案为:10-4.2。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和 去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法不正确的是
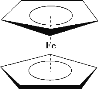
A.1mol 环戊二烯( ![]() )中含有σ键的数目为1NA
)中含有σ键的数目为1NA
B.环戊二烯中碳原子的杂化方式有 sp3 和 sp2
C.二茂铁属于分子晶体
D.二茂铁分子中的化学键有极性共价键、非极性共价键和配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池可净化废水,同时还能获得能源或有价值的化学产品,图1为其工作原理,图2为废水中Cr2O72-浓度与去除率的关系。下列说法不正确的是( )
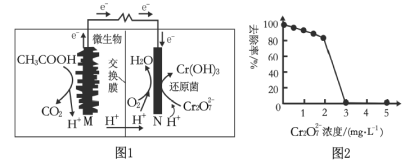
A.图1燃料电池工作一段时间后,N极附近的溶液pH增大
B.外电路转移2 mol电子时,N极消耗标准状况下11.2 L O2
C.图2中Cr2O72-浓度较大时,其去除率下降可能是Cr2O72-浓度较大造成还原菌失活所致
D.M极为电池负极,发生的电极反应为CH3COOH+2H2O-8e-=2CO2↑+8H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下的反应为SO2(g)+![]() O2(g)
O2(g)![]() SO3(g) △H=-98 kJ·mol-1。开始时在100 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出热量196 kJ,此温度下,该反应的平衡常数为
SO3(g) △H=-98 kJ·mol-1。开始时在100 L的密闭容器中加入4.0 mol SO2(g)和10.0 mol O2(g),当反应达到平衡时共放出热量196 kJ,此温度下,该反应的平衡常数为
A.1B.3C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量)。
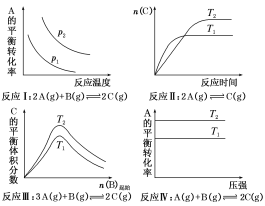
根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:ΔH>0,p2>p1B.反应Ⅱ:ΔH<0,T1<T2
C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1D.反应Ⅳ:ΔH<0,T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙两个容积相同的密闭容器,分别充入NH3和N2,当它们的温度和密度都相同时,下列说法中正确的是( )
A.两容器气体的质量相等B.两容器气体所含分子数相等
C.两容器气体所含原子数相等D.两容器中气体的压强相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A. 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B. NCl3分子是非极性分子
C. NBr3比NCl3易挥发
D. 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I.摩擦剂中氢氧化铝的定性检验取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是________。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是_______。
II.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
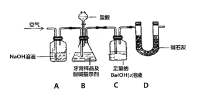
依据实验过程回答下列问题:
(3)D装置的作用是__________。
(4)下列各项措施中,不能提高测定准确度的是__________(填标号)。
①在加入盐酸之前,应排净装置内的CO2气体
②滴加盐酸不宜过快
③在A-B之间增添盛有浓H2SO4的洗气装置
④在B-C之间增添盛有饱和NaHCO3溶液的洗气装置
(5)实验中准确称取10.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①BaCl2、②金刚石、③醋酸钠、④Na2SO4、⑤干冰、⑥碘六种物质,按下列要求回答问题:
(1)熔化时不需要破坏化学键的是______(填序号,下同),熔化时需要破坏共价键的是______,熔点最高的是______,熔点最低的是______。
(2)属于离子晶体的是______(填序号,下同),只含有离子键的物质是______。
(3)①的电子式是______,⑤的电子式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com