
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:

⑴ 在提取碘的过程中有关实验的操作名称:① ,③ ;写出过程②中有关反应的化学方程式: 。
⑵提取碘的过程中,可供选择的有机试剂是 。
A.酒精 B.苯 C.乙酸 D.四氯化碳
⑶为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是 。
⑷从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏。指出如图所示实验装置中的错误之处: ; ; 。

【答案】30、⑴过滤,萃取;2I-+Cl2===2Cl-+I2 ⑵BD ⑶分液漏斗
⑷①缺少石棉网;②温度计的水银球插到液面以下;③冷凝管中进出水方向颠倒
【解析】
试题分析:(1)过程①是分离不溶性物质和溶液,用过滤的操作;因为碘在有机溶剂中的溶解度较大,而在水中的溶解度较小,分离碘和水的溶液用萃取、分液的方法,所以过程③是萃取。氯气能将I-氧化成碘单质,所以过程②反应的化学方程式为2I-+Cl2===2Cl-+I2。
(2)萃取是利用溶质在不同溶剂中溶解度的不同而分离的,提取碘的过程用萃取的方法,选取萃取剂的标准是①溶质在萃取剂中的溶解度比在原溶剂中要大,②萃取剂与原溶剂不相溶,③萃取剂与溶质不反应,答案选BD。
(3)海藻灰中碘离子转化为碘的有机溶液采取萃取分液的方法,分液必须用到分液漏斗。
(4)该装置是蒸馏操作装置,该实验装置中的错误之处有①缺少石棉网;②温度计的水银球插到液面以下;③冷凝管中进出水方向颠倒。


科目:高中化学 来源: 题型:
【题目】工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:

已知: Cu2O + 2H+ = Cu + Cu2+ + H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 。
(2)反应Ⅰ完成后,铁元素的存在形式为 。(填离子符号)请写出生成该离子的离子方程式 。
(3)x、y对应的数值范围分别是 、 。
(4)电解法获取Cu时,阴极反应式为 ,阳极反应式为 。
(5)下列关于NaClO调pH的说法正确的是 。
a. 加入NaClO可使溶液的pH降低
b. NaClO能调节pH的主要原因是由于发生反应ClO-+ H+![]() HClO, ClO-消耗H+,从而达到调节pH的目的
HClO, ClO-消耗H+,从而达到调节pH的目的
c .NaClO能调节pH的主要原因是由于NaClO水解ClO-+ H2O![]() HClO+OH-,OH-消耗H+ ,从而达到调节pH的目的
HClO+OH-,OH-消耗H+ ,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为_________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组利用如图给定的仪器组成一套实验装置(各仪器只允许用一次),在室温、 1.01×105 Pa的条件下测定镁的相对原子质量。
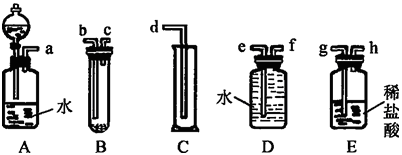
请回答下列问题:
(1)假设气流方向为左→右,则各仪器的接口连接的先后顺序为 (用小写字母填写)。
(2)连接好仪器后,要进行的操作有以下几步:
①待仪器B中的物质恢复至室温时,测量量筒 C中水的体积(假定将测定的体积换算成标准状况下为 V mL);
②擦掉镁条表面的氧化膜,将其置于天平上称量(假定其质量为m g,并将其放入试管B中);
③检查各装置的气密性;
④旋开仪器A上分液漏斗的活塞,当镁条完全溶解时再关闭活塞。
上述几步操作的先后顺序是 。
(3)根据实验数据可计算出镁的相对原子质量,其数学表达式为 。
(4)若未将试管B冷却至室温就测量量筒C中水的体积,这将会使所测镁的相对原子质量数据 (填“偏大”“偏小”或“无影响”)。
(5)若未擦净镁条表面的氧化膜就进行实验,这将会使所测镁的相对原子质量数据 (填“偏大”“偏小”或“无影响”)。
(6)实验中需要用480 mL 1 mol/L的盐酸,配制过程中用于定容的玻璃仪器的规格和名称是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期中的两种元素X和Y,X的原子序数大于Y,X原子的最外层电子数是内层电子总数的一半,Y的二价阴离子和Ne原子的电子层结构相同,关于X和Y形成的化合物Z的说法正确的是
A. Z是酸性氧化物 B. Z的水化物是碱
C. Z的化学式为X2Y D. Z的水化物的酸性强于硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的说法中,正确的是( )
A. 苯不能使酸性KMnO4溶液退色,属于饱和烃
B. 常温下苯是一种易溶于水且密度比水小的液体
C. 苯不具有典型的双键,故苯不能发生加成反应
D. 苯分子为平面正六边形结构,6个碳原子之间的价键完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应” 的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有 熔融物落人沙中”。査阅《化学手册》知,Al、Al2O3、Fe、Fe2O3的熔、沸点数据如下:
物质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2 054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 | — |
I.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理:________(填“合理”或“不合理”)。
(2)设汁一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是________,反应的离子方程式为___________。
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。若铁被氧化为Fe3+,在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
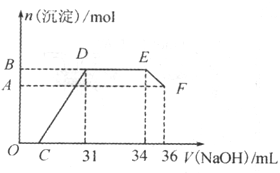
回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为____________。在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为____________。
(2)B与A的差值为_________mol。B点对应的沉淀的物质的量为___________mol,C点对应的氢氧化钠溶液的体积为____________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在塑料袋中放一个成熟的苹果,再放些青香蕉,将袋口密封。两天后,发现青香蕉成熟了。导致青香蕉成熟的物质是成熟苹果释放出的 ( )
A.C2H4 B.CH3COOH C.C6H6 D.CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 共价化合物中可能含有离子键
B. Ca2+、K+、Cl﹣、S2﹣四种粒子的离子半径依次减小
C. ![]() Po、
Po、![]() Po、
Po、![]() Po三种原子的核外电子数分别为124、125、126
Po三种原子的核外电子数分别为124、125、126
D. 第ⅥA族元素氧、硫、硒对应的氢化物H2O、H2S、H2Se的稳定性依次减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com