
| A. | 聚丙烯的结构简式: | B. | 乙醇的结构式:CH3CH2OH | ||
| C. | 四氯化碳分子的电子式为: | D. | 丙烷分子的球棍模型为: |
分析 A.聚丙烯是由丙烯不饱和的碳原子相互加成得到的,注意原子之间连接.
B.结构式中需要用短线代替所有的共用电子对;
C.四氯化碳的电子式中漏掉了氯原子的最外层6个电子;
D.丙烷为含有3个碳的烷烃,碳原子半径大于H原子.
解答 解:A.聚丙烯是由丙烯不饱和的碳原子相互加成得到的,其结构简式为 ,故A错误;
,故A错误;
B.CH3CH2OH为乙醇的结构简式,乙醇的结构式为: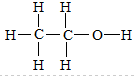 ,故B错误;
,故B错误;
C.氯原子未成键的孤对电子对未标出,四氯化碳电子式为 ,故C错误;
,故C错误;
D.丙烷分子中,碳原子半径大于氢原子,其球棍模型为: ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、球棍模型、结构式、结构简式等知识,明确常见化学用语的书写原则为解答关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A1Cl3、NH3•H20 | B. | ZnCl2、NH3•H20 | C. | A1Cl3、NaOH | D. | ZnCl2、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{64m}{n}$ | B. | $\frac{32m}{n}$ | C. | $\frac{n}{32m}$ | D. | $\frac{n}{64m}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是我校实验室化学试剂浓硫酸标签上的部分内容.现需要480mL 1mol•L-1的稀硫酸.用该浓硫酸和蒸馏水配制,可供选用的仪器有:①胶头滴管;②玻璃棒;③烧杯;④量筒.
如图是我校实验室化学试剂浓硫酸标签上的部分内容.现需要480mL 1mol•L-1的稀硫酸.用该浓硫酸和蒸馏水配制,可供选用的仪器有:①胶头滴管;②玻璃棒;③烧杯;④量筒.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+ | B. | Na+ | C. | CO32- | D. | Ba2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com