
| A. | A1Cl3、NH3•H20 | B. | ZnCl2、NH3•H20 | C. | A1Cl3、NaOH | D. | ZnCl2、NaOH |
分析 与量无关的反应,改变滴定顺序反应现象相同,不能鉴别;而与量有关的反应,改变滴定顺序,现象不同可鉴别,以此来解答.
解答 解:A.改变滴加顺序,均生成白色沉淀,不能鉴别,故A选;
B.氨水少量生成白色沉淀,氨水过量不生成沉淀,则改变滴加顺序,现象不同,能鉴别,故B不选;
C.NaOH少量生成白色沉淀,NaOH过量不生成沉淀,则改变滴加顺序,现象不同,能鉴别,故C不选;
D.NaOH少量生成白色沉淀,NaOH过量不生成沉淀,则改变滴加顺序,现象不同,能鉴别,故D不选;
故选A.
点评 本题考查混合物的检验和鉴别,为高频考点,侧重于考查学生分析能力、实验能力,注意把握与量有关的离子反应及现象,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
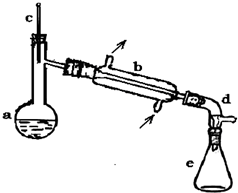 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应 和实验装置如图:
和实验装置如图:| 相对分子质量 | 密度/(g?cm-3 ) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活性炭、氯气都能使品红溶液褪色 | |
| B. | 苯、乙醇、纤维素都能与浓硝酸反应 | |
| C. | 乙烯、氯乙烯都能使溴水褪色 | |
| D. | 淀粉、蛋白质都能发生显色(或颜色)反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1 mol水的体积约为22.4L | |
| B. | 只有在标准状况下,气体的摩尔体积才是22.4mol/L | |
| C. | 在标准状况下,1molH2和O2的混合气体体积约为22.4 L | |
| D. | 任何条件下,气体的摩尔体积都是22.4L/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚丙烯的结构简式: | B. | 乙醇的结构式:CH3CH2OH | ||
| C. | 四氯化碳分子的电子式为: | D. | 丙烷分子的球棍模型为: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于0.6 mol | B. | 等于1 mol | ||
| C. | 大于0.6 mol,小于1 mol | D. | 大于1 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com