
| �Ҵ� | ������ | �� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | �����ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 1.44 | 3.1 |
| �е�/�� | 78.5 | 38.4 | 59 |
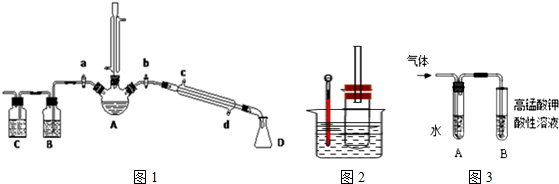
���� ��1��������Ӧ���¿ڽ�ˮ���Ͽڳ�ˮ���Ա�֤ˮ���������ܣ�������������ã�����������ˮ���ķ����������������෴����ֱ�����ܵ�����Ϊ�����������ã�
��2��Ũ�������ǿ�����ԣ����Խ�����������Ϊ�嵥�ʣ�Ϊ�˸��õĿ����¶ȣ������ˮԡ���ȵķ�����
��3���������Ȼ�̼�г�ȥ�壬��������������Һ����HBr��
��4����Һ���������л����壬����ʱע���������������ʽǶȿ��ǣ�������е�ͣ����Բ����������룻
��5�������鲻����ˮ���Ҵ�����ˮ��
��6���Ҵ����л�ԭ�ԣ���ʹ���������ɫ������ϩ�ļ�����ɸ��ţ��Ҵ�����ˮ����Ӧ����ϩ����ˮ�����ӳɷ�Ӧʹ��ˮ��ɫ��
��� �⣺��1����������ˮ���ķ����������������෴��������ʹ����ˮ���������ܣ����ܳ��������������ֱ����������ˮ�����¿ڽ����Ͽڳ����Ҵ��ӷ�����ֱ���������������������ã�ʹ�Ҵ�������������ƿ�м�����Ӧ��
�ʴ�Ϊ���£��ϣ�����������
��2��Ũ�������ǿ�����ԣ����Խ�����������Ϊ�嵥�ʣ��óȺ�ɫ���ʿ�����Br2��Ϊ�˸��õĿ��Ʒ�Ӧ�¶ȣ�Ӧ��ȡ�ļ��ȷ�ʽ��ˮԡ���ȣ�
�ʴ�Ϊ��Br2��ˮԡ���ȣ�
��3��B��ʢ�����Ȼ�̼�г�ȥ�壬C��ʢ����������Һ����HBr���ɣ�
�ʴ�Ϊ�����Ȼ�̼����������Һ��
��4������ȥ�������е���������Br2����
A��Na2SO3���巢��������ԭ��Ӧ��Na2SO3�ɳ�ȥ�壬��A��ȷ��
B�������������е��ܽ�ȱ���ˮ�д�ˮ���Գ�ȥ�������е��壬��B����
C������������Һ��ʾ���ԣ����Գ�ȥ�����壬��������Ҳ���ڴ���Һ���ˮ�ⷴӦ����C����
D����������鶼���������Ȼ�̼�����ܽ����߷��룬��D����
������ķе���38.4�棬�ʲ�������������룬
�ʴ�Ϊ���£�����
��5�������鲻����ˮ��������������Һ��Ϻ�ֲ㣬�������ڼ���������ˮ�������Ҵ����廯�ƣ����߶�������ˮ�����Һ�岻�ֲ㣬˵����������NaOH��Һ����ȫ��Ӧ��
�ʴ�Ϊ��Һ�岻�ֲ㣻
��6���Ҵ����л�ԭ�ԣ���ʹ���������ɫ��Ϊ��ֹ�Ҵ�����ϩ����ĸ��ţ�Ӧ��A�����Ҵ��������������ɫ����֤����ϩ�Ĵ��ڣ�˵��֤����������NaOH�Ҵ���Һ�з���������ȥ��Ӧ��
�Ҵ�����ˮ����Ӧ����ϩ����ˮ�����ӳɷ�Ӧʹ��ˮ��ɫ������A�Թܣ�B�Թ��е��Լ�ӦΪ��ˮ�������ˮ��ɫ����֤����ϩ�Ĵ��ڣ�˵��֤����������NaOH�Ҵ���Һ�з���������ȥ��Ӧ��
�ʴ�Ϊ�������Ҵ�����ˮ��
���� ���⿼����±���������ʣ�±������ȡ����Ӧ����ȥ��Ӧ���Ǹ߿������ſ��㣬���л��ϳ�����ʵ�ֹ�����ת������Ҫ��Ӧ��ע��������Ӧ����������������ص㣬����ѧ���������⣬��������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢ� | B�� | �� | C�� | �ڢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
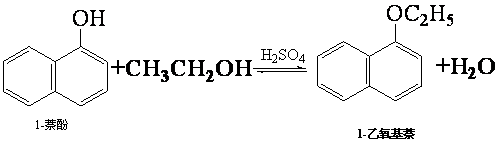
| ���� | ��Է� ������ | ״̬ | �۵㣨�棩 | �е㣨�棩 | �ܽ�� | |
| ˮ | �Ҵ� | |||||
| 1-���� | 144 | ��ɫ���ɫ���νᾧ���ĩ | 96�� | 278�� | ����ˮ | �������Ҵ� |
| 1-�������� | 172 | ��ɫҺ�� | 5.5�� | 267�� | ������ˮ | �������Ҵ� |
| �Ҵ� | 46 | ��ɫҺ�� | -114.1�� | 78.5�� | ����Ȼ��� | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ�����������뷴Ӧ�����ֵ����� | |
| B�� | �����¶ȣ����Ըı仯ѧ��Ӧ�ķ�Ӧ�� | |
| C�� | ��H�Ĵ�С���Ȼ�ѧ����ʽ�еĻ�ѧ�������� | |
| D�� | 1 mol H2������Cl2����ȫȼ�����ų�����������H2��ȼ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������������������ֱ���ȫȼ�գ����߷ų��������� | |
| B�� | ��C��ʯī��s���TC�����ʯ��s����H=+11.9 kJ/mol��֪�����ʯ��ʯī�ȶ� | |
| C�� | ��֪��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l������H=-57.3 kJ/mol��������0.5mol H2SO4��Ũ�����뺬1 mol NaOH��ϡ��Һ��ϣ��ų�����������57.3 kJ | |
| D�� | ����ı�ȼ����Ϊ890.3kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2 O2��g���TCO2��g��+2H2O ��g����H=-890.3kJ•mol-1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com