
【题目】25℃时,pH=2的HCl溶液中,由水电离出的H+浓度是
A. 1.0×10-2molL-1 B. 1.0×10-7molL-1
C. 1.0×10-12molL-1 D. 1.0×10-14molL-1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,1570C时开始分解:
(1)探究草酸的酸性
250C H2C2O4 K1 = 5.4 x 10-2,K2 = 5. 4 x 10 -5 ;H2CO3 K1=4.5x10-7 K2= 4.7X10-11
下列化学方程式可能正确的是________
A. H2C2O4 +CO32-=HCO3- +HC2O4- B. HC2O4- +CO32-= HCO3-+C2O42-
C. 2C2O42-+CO2+H2O=2HC2O4-+CO32- D. H2C2O4 +CO32-=C2O42-+H2O+CO2
(2)探究草酸分解产物
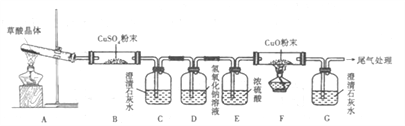
①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:_______,证明有CO气体生成的现象是:_____________________
②写出H2C2O4分解的化学方程式_____________________
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加人4mLO.O1mol/T. KMnO4酸性溶液和2mL O.1mol/L H2C2O4溶液, 再向乙试管中加人一粒黄豆大的MnSO4固体,摇匀。填写下表:
反应现象 | ______________ |
实验结论 | ______________ |
试管中发送反应的离子方程式 | ______________ |
(4)用酸性KMnO4溶液滴定Na2C2O4求算Na2C2O4的纯度
实验步骤:准确称取2.OgNa2C2O4固体,配成1OO mL溶液,取出20.OOmL于锥形瓶中=再向瓶 中加人足量稀H2SO4 ,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.OOmL0
①高锰酸钾溶液应装在_______滴定管中。(填“酸 式”或“碱 式”)
②滴定至终点时的实验现象是:______________。
③Na2C2O4的纯度是:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法正确的是
A. 元素周期表是按照元素相对原子质量大小排列而成的
B. 元素周期表有7个横行,也是7个周期;有18个纵行,即18个族
C. 凡是位于元素周期表中同一周期的元素,都是按从左到右的顺序原子最外层电子数由1递增到8
D. 凡是位于元素周期表中同一主族的元素,都是按从上到下的顺序电子层数逐渐增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空:某化学小组拟采用如下装置(夹持和加热仪器等已略去)来电解饱和食盐水,并用电解产生的 H2 还原 CuO 粉末来测定 Cu 的相对原子质量,同时验证氯气的氧化性。

完成下列填空:
(1) 写出甲装置中反应的化学方程式______________________________。
(2) 为完成上述实验,正确的连接顺序为 A 连______,B连_____(填写接口字母)。
(3)乙装置中 a 试剂可以是_______________。
(4) 测定 Cu 的相对原子质量。将w g CuO 置于硬质玻璃管中,按以下两个方案测得的数据计算 Cu 的相对原子质量
方案 1 | 方案 2 | |
U 型管+固体 | 硬质玻璃管+固体 | |
反应前的总质量/g | a | c |
反应后的总质量/g | b | d |
你认为较佳方案是_____________,另一个方案得到的 Cu 的相对原子质量会_______(选填“偏低”、或“偏高”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中,微粒的物质的量浓度关系正确的是
A. 0.1 mol·L-1 pH<7的NaHSO3溶液中:c(HSO)>c(H2SO3)>c(SO![]() )
)
B. 10 mL 0.5 mol·L-1 CH3COONa溶液与10 mL 1 mol·L-1盐酸混合:c(Cl-)>c(H+)>c(Na+)>c(CH3COO-)>c(OH-)
C. 在NaHCO3溶液中一定有:c(Na+)+c(H+)=c(HCO)+c(OH-)+c(CO![]() )
)
D. c(NH)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:c[(NH4)2CO3]<c[(NH4)2SO4]<c(NH4Cl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中可大量共存,并能形成无色溶液的一组是( )
A.H+、Ba2+、NO3-、I-
B.Ba2+、Cu2+、NO3-、SO42-
C.Mg2+、Na+、OH-、MnO4-
D.K+、Na+、OH—、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
主族周期 | I A | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为_______。元素⑩在周期表中的位置为________________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_________,碱性最强的化合物的电子式是_______,⑤的单质在该化合物的水溶液中反应的离子方程式为_____。
(3)用电子式表示元素④与⑥的化合物的形成过程___________________,该化合物属于_____(填“共价”或“离子”)化合物。
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是_____(用化学式表示)。
(5)元素①的最简单氢化物的结构式为________,与该化合物相差一个CH2的同系物可用于形成燃料电池,写出电解质溶液呈碱性时负极的电极反应式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化锂是制取锂和锂的化合物的原料,用电解法制备氢氧化锂的工作原理如下图所示,下列叙述不正确的是
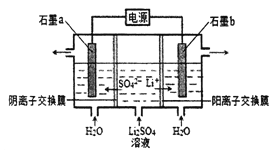
A. b极附近溶液的pH增大
B. a极反应为2H2O-4e-= O2↑+4H+
C. 该法制备LiOH还可得到硫酸和H2
D. 当电路中通过1mol 电子时,有2mol LiOH生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com