
【题目】在含有酚酞的0.1 molL-1氨水中加入少量的NH4Cl晶体,则溶液颜色
A. 变浅 B. 变深 C. 变蓝 D. 不变
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】实验室用下图装置制取少量溴苯,试填写下列空白。

(1)请写出仪器名称,a__________、 d __________,在烧瓶a中装的试是__________、__________、_________。
(2)请你推测长直导管b的作用:一是_____________________________,二是____________________________________的作用。
(3)请你分析导管c的下口可否浸没于液面中?为什么?____________________________________
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液有________生成,此现象说明这种获得溴苯的反应属于:____________________。(填有机反应类型)
(5)课本采用如下装置进行实验,请在图中标出冷凝水流动方向______(上或下)口进________(上或下)口出。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.10mol/L HA(Ka=10-9.89)溶液,调节溶液pH后。保持[HA] + [A-]=0.10mol/L。下列关系正确的是
A. pH=2.00时,[HA] > [H+]> [OH-] > [A-]
B. pH=7.00时,[HA] = [A-] > [OH-]= [H+]
C. pH=9.89时,[HA] = [A-] > [OH-]> [H+]
D. pH=14.00时,[OH-]>[A-]>[H+]>[HA]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2NO2(g)![]() 2NO(g)+O2(g)在恒容密闭容器中进行,达到平衡状态的标志是
2NO(g)+O2(g)在恒容密闭容器中进行,达到平衡状态的标志是
①单位时间内生成n molO2的同时生成2n mol NO
②单位时间内生成n molO2的同时生成2n mol NO2
③用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态.
A. ①③⑤ B. ②④⑥ C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是__________
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2==4CuSO4+2 H2O,当1mol O2发生反应时,还原剂所失电子的物质的量为___mol。向CuSO4溶液中加入镁条时有气体生成,该气体是____。
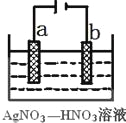
(3)右图为电解精炼银的示意图,_____(填a或b)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为____________。
(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,pH=2的HCl溶液中,由水电离出的H+浓度是
A. 1.0×10-2molL-1 B. 1.0×10-7molL-1
C. 1.0×10-12molL-1 D. 1.0×10-14molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯(![]() )是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
)是生产各种塑料的重要单体,可通过乙苯催化脱氢制得: ![]() ΔH=Q kJ/mol。在实际生产中,常保持总压0.1MPa 不变,并向反应体系中加入稀释剂,如CO2、N2等(不参与反应)。乙苯(EB) 脱氢转化率与反应混合气物质的量之比及反应温度的关系如图所示。下列说法正确的是
ΔH=Q kJ/mol。在实际生产中,常保持总压0.1MPa 不变,并向反应体系中加入稀释剂,如CO2、N2等(不参与反应)。乙苯(EB) 脱氢转化率与反应混合气物质的量之比及反应温度的关系如图所示。下列说法正确的是

A. 相同条件下,正反应速率: v(A) >v(B)
B. 若在恒容条件下加入稀释剂(N2),能增大乙苯的转化率
C. 若A点乙苯的转化率为60%,则混合气体中苯乙烯的37.5 %
D. 用平衡分压来代替平衡浓度计算,其中分压=总压×物质的量分数,则600℃时,B点的平衡常数Kp=0.019MPa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】规律提炼题组
完成下列与溶液pH有关的计算,并提炼解题规律。
(1)室温下pH=4的NH4Cl溶液和HCl溶液中由水电离出的c(H+)之比为_______
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后,溶液中的氢离子浓度为 _____
(3)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合:,
①若所得混合溶液为中性,则a:b= ____
②若所得混合溶液pH=3,则a:b=_____
(4)已知某温度时0.1 molL-1NaOH pH等于11,在此温度下,若将100体积pH1=a的H2SO4溶液与1体积pH2=b的NaOH溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是________________(用含a、b的表达式表示)
(5)(学法题)总结归纳求混合溶液pH时,应注意的问题:__________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com