
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是
A. 9 g超重水(3H216O)含中子数为6NA
B. 0.1 molH2和0.1 mol I2于密闭容器中充分反应后,其分子总数为0.2 NA
C. 1 L 0.1 mol·L-1的NaHCO3溶液中![]() 和
和![]() 离子数之和为0.1 NA
离子数之和为0.1 NA
D. 235g核素![]() 发生裂变反应:
发生裂变反应: ![]() 净产生的中子(
净产生的中子(![]() )数为10NA
)数为10NA
【答案】B
【解析】A项,超重水的摩尔质量为22g/mol,n(3H216O)=![]() =
=![]() mol,1个3H216O中含有12个中子,9 g超重水含中子数为
mol,1个3H216O中含有12个中子,9 g超重水含中子数为![]() 12NA=
12NA=![]() NA,错误;B项,H2与I2发生反应:H2+I2
NA,错误;B项,H2与I2发生反应:H2+I2![]() 2HI,该反应反应前后分子数不变,充分反应后分子物质的量仍为0.2mol,分子总数仍为0.2NA,正确;C项,n(NaHCO3)=0.1mol/L
2HI,该反应反应前后分子数不变,充分反应后分子物质的量仍为0.2mol,分子总数仍为0.2NA,正确;C项,n(NaHCO3)=0.1mol/L![]() 1L=0.1mol,HCO3-在溶液中既存在电离平衡(HCO3-
1L=0.1mol,HCO3-在溶液中既存在电离平衡(HCO3-![]() H++CO32-)又存在水解平衡(HCO3-+H2O
H++CO32-)又存在水解平衡(HCO3-+H2O![]() H2CO3+OH-),根据碳原子守恒,溶液中CO32-、HCO3-和H2CO3三者之和为0.1NA,错误;D项,n(
H2CO3+OH-),根据碳原子守恒,溶液中CO32-、HCO3-和H2CO3三者之和为0.1NA,错误;D项,n(![]() )=
)=![]() =1mol,根据裂变反应,净产生9mol中子,错误;答案选B。
=1mol,根据裂变反应,净产生9mol中子,错误;答案选B。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】欲配制250mL0.1molL﹣1的H2SO4溶液,回答下列有关问题,有如下操作步骤:
①把量取好的浓H2SO4沿烧杯壁缓缓倒入盛有一定量水的小烧杯中,并用玻璃棒不断搅拌
②把①中所得溶液小心转入仪器A中
③继续向A中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入A中,并轻轻摇匀
⑤用玻璃塞将A塞紧,充分摇匀
请填写下列空白: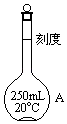
(1)写出图中仪器A的名称 , 使用此仪器A前应检查它是否 .
(2)操作步骤的正确顺序为(填序号) .
(3)转移溶液时,应先将溶液 , 然后将溶液沿玻璃棒注入仪器A中.
(4)若出现下列操作时,对所配溶液浓度将有何影响(填“偏高、偏低、无影响”)
①量筒用蒸馏水冼净后,再量取浓硫酸;
②不将洗涤液转移入仪器A就定容;
③定容时,仰视仪器A刻度线;
④仪器A只用蒸馏水洗涤,但未经干燥而配制溶液 .
(5)若实验过程中出现如下情况应如何处理?
①加蒸馏水时不慎超出了刻度;
②向容量瓶中转移溶液时,不慎有液滴掉在容量瓶外面 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不合理的是( )
A. 可以用酸性高锰酸钾除去甲烷中的乙烯
B. 分离苯和硝基苯的混合物,可用蒸馏法
C. 可用氢氧化钠溶液将溴苯中的溴除去
D. 可用水来鉴别苯、乙醇、四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸盐(NaClO2)可作漂白剂,在常温下不见光时可保存一年,但在酸性溶液里因生成
亚氯酸而发生分解:5HClO2=4ClO2↑+H++Cl-+2H2O。分解时,刚加入硫酸,反应缓慢,随后突然反应释放出大量 ClO2,这是因为
A. 酸使亚氯酸的氧化性增强
B. 溶液中的 H+起催化剂的作用
C. 溶液中的 Cl-起催化剂的作用
D. 逸出的 ClO2 使反应的生成物的浓度降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行X2(气)+ 3Y2(气)![]() 2Z(气)的反应,其X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.2mol/L,当反应达平衡时,浓度分别是a、b、c(mol/L),回答:
2Z(气)的反应,其X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.2mol/L,当反应达平衡时,浓度分别是a、b、c(mol/L),回答:
①各物质的浓度有可能的是___________.
A.c=0.5mol/L B.b=0.5mol/L C.c=0.4mol/L D.a=0.3mol/L
②若a=_____________________时,b=0.15mol/L。
③a、b的取值必须满足的一般条件是_______________________.
④a的取值范围是:_____________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6mol/L。向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积变化忽略不计)
A. 0.225mol/L B. 0.30mol/L C. 0.36mol/L D. 0.45mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,隔板I固定不动,活塞II可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)![]() xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )
xC(g),向M、N中通入1mol和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是( )

A. 若x=3,达到平衡后A的体积分数关系为:![]()
B. 若x<3,C的平衡浓度关系为:c(M)<c(N)
C. 若x>3,达到平衡后B的转化率关系为:![]()
D. x不论为何值,平衡时M、N中的平均相对分子质量都相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室进行二氧化硫制备与性质实验的组合装置如图所示,部分夹持装置未画出。

请回答下列问题:
(1)检验装置A气密性的方法是关闭弹簧夹1、2,向分液漏斗中加入水,然后打开活塞,____________________ ,则气密性良好。
(2)为检验SO2与Na2O2的反应是否有氧气生成,装置B中盛放的试剂X应为________,装置D中碱石灰的作用是______________________________________。
(3)制取SO2时不用98%浓硫酸的原因是___________________。
(4)关闭弹簧夹2,打开弹簧夹1,注入70%的硫酸至浸没三颈烧瓶中的固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是___________________________。
(5)关闭弹簧夹1,打开弹簧夹2,残余气体进入装置E、F、G中,能说明I-的还原性弱于SO2的现象为_____________,发生反应的离子方程式是__________________。
(6)为了验证装置E中SO2与FeCl3发生了氧化还原反应,某学生设计了如下实验:取少量装置E中的溶液于试管中,向其中加入稀硝酸酸化的BaCl2溶液,产生白色沉淀,并由此判断SO2与FeCl3发生了氧化还原反应。上述方案是否合理?________(填“合理”或“不合理”),原因是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com