
| A、除硫酸厂尾气:SO2+2NH3+H2O═(NH4)2SO3 | ||||
| B、消除硝酸工业尾气氮氧化物的污染:2NaOH+NO2+NO═2NaNO2+H2O | ||||
C、制备CuSO4:Cu+2H2SO4(浓)
| ||||
D、制备CuSO4:2Cu+O2
|


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、反应速率减慢,产生H2的量不变 |
| B、反应速率加快,产生H2的量不变 |
| C、反应速率不变,产生H2的量略增加 |
| D、反应速率加快,产生H2的量略减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应说明钠是强氧化剂,可用于冶炼金属 |
| B、该反应条件是TiCl4在熔融状态或水溶液中 |
| C、Ti是氧化产物 |
| D、若有1mol TiCl4参加反应,则转移的电子为4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
131 53 |
127 53 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
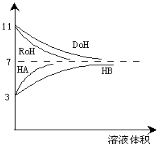
查看答案和解析>>
科目:高中化学 来源: 题型:


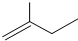
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com