
【题目】氮的氧化物和硫的氧化物是主要的大气污染物,烟气脱硫脱硝是环境治理的热点问题。回答下列问题:
(1)目前柴油汽车都用尿素水解液消除汽车尾气中的NO,水解液中的NH3将NO还原为无害的物质。该反应中氧化剂与还原剂物质的量之比为___。
(2)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO42-。
①KMnO4脱硫(SO2)的离子方程式为___。
②加入CaCO3的作用是___。
③KMnO4/CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为___。
(3)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液pH对脱硫脱硝的影响如图所示:
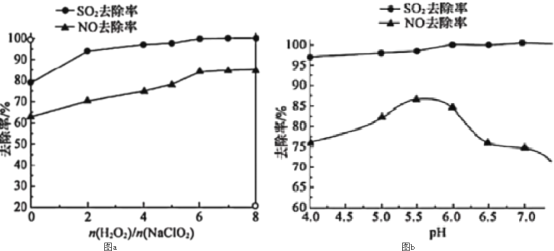
图a和图b中可知脱硫脱硝最佳条件是___。图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因是___。
【答案】2:3 SO2 +2MnO4-+2H2O === SO42- + 2MnO42- + 4H+ 消耗脱硫过程中的氢离子,有利于平衡正向移动 1:1 n(H2O2):n(NaClO2) = 6:1,pH值在5.5—6.0 可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱
【解析】
⑴根据氧化还原反应得出氧化剂和还原剂的比例关系。
⑵根据氧化还原反应原理写离子方程式,生成的氢离子和碳酸钙反应,消耗氢离子,利于平衡正向移动,根据比例关系得出高锰酸钾和碳酸钙的比例。
⑶根据图像信息得出脱硫脱硝最佳条件,用氧化还原反应的强弱随pH变化的影响分析减弱的原因。
⑴水解液中的NH3将NO还原为无害的物质氮气,根据氧化还原反应原理,氨气化合价升高3个价态,为还原剂,NO化合价降低2个价态,为氧化剂,根据升降守恒配平原理,因此氨气前配2,NO前面配系数3,因此该反应中氧化剂与还原剂物质的量之比为2:3,故答案为:2:3。
⑵①KMnO4脱硫(SO2)反应生成锰酸根和硫酸根,离子方程式为SO2 +2MnO4-+2H2O === SO42- + 2MnO42- + 4H+,故答案为:SO2 +2MnO4-+2H2O === SO42- + 2MnO42- + 4H+。
②反应过程中生成了硫酸,加入CaCO3的作用是消耗脱硫过程中的氢离子,有利于平衡正向移动,故答案为:消耗脱硫过程中的氢离子,有利于平衡正向移动。
③2molKMnO4反应生成4mol氢离子,4mol氢离子消耗2mol碳酸钙,因此CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为1:1,故答案为1:1。
⑶根据图中的转化率和去除率关系,可知脱硫脱硝最佳条件是n(H2O2):n(NaClO2) = 6:1,pH值在5.5—6.0;NO在pH>5.5时可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱,故答案为:n(H2O2):n(NaClO2) = 6:1,pH值在5.5—6.0;可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收Cu并制备ZnO的部分实验过程如图所示:
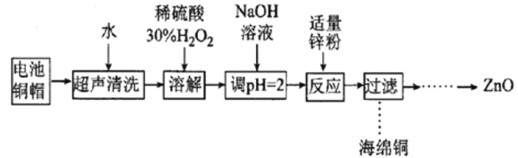
下列叙述错误的是
A. 合理处理废弃旧电池的铜帽既有利于节约资源,又有利于保护环境
B. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2
C. 加入锌粉反应的离子为Cu2+
D. “过滤”操作后直接将溶液蒸发结晶、高温灼烧得到ZnO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铜银合金(含少量铁)废料为原料回收银和铜的工艺流程如下:

下列说法正确的是
A. 粗铜溶于过量稀硝酸,过滤、低温干燥得纯铜
B. 电解时用粗银作阴极,硝酸银溶液为电解质溶液
C. 用稀硫酸处理渣料时主要发生了氧化还原反应
D. 从滤液B中可以提取绿矾(FeSO4·7H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2(g)+3H2(g)![]() 2NH3(g)反应过程中能量变化如图所示,下列有关叙述正确
2NH3(g)反应过程中能量变化如图所示,下列有关叙述正确
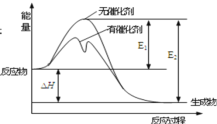
A.该反应正反应的活化能小于逆反应的活化能
B.该反应的逆反应为放热反应
C.使用催化剂使该反应的反应热发生改变
D.该反应的ΔH=E2-E1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,A、B、C、D为短周期主族元素,其中A、B、C在周期表中所处的位置如图所示,且它们的质子数之和为32。D元素原子的最外层电子数为次外层电子数的2倍。下列说法正确的是

A.原子半径:D>A>CB.常温常压下,B单质为固态
C.气态氢化物热稳定性:B>CD.C的最高价氧化物的水化物是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对KSCN的性质进行探究,设计如下实验:

(1)①用离子方程式表示实验I溶液变红的原因___。
②针对实验I中红色褪去的原因,小组同学认为是SCN-被酸性KMnO4氧化为SO42-,并设计如图实验装置证实了猜想是成立的。

其中X溶液是___,检验产物SO42-的操作及现象是___。
(2)针对实验II“红色明显变浅”,实验小组提出预测。
原因①:当加入强电解质后,增大了离子间相互作用,离子之间牵制作用增强,即“盐效应”。“盐效应”使Fe3++SCN-![]() [Fe(SCN)]2+平衡体系中的Fe3+跟SCN-结合成[Fe(SCN)]2+的机会减少,溶液红色变浅。
[Fe(SCN)]2+平衡体系中的Fe3+跟SCN-结合成[Fe(SCN)]2+的机会减少,溶液红色变浅。
原因②:SCN-可以与Fe2+反应生成无色络合离子,进一步使Fe3++SCN-![]() [Fe(SCN)]2+平衡左移,红色明显变浅。
[Fe(SCN)]2+平衡左移,红色明显变浅。
已知:Mg2+与SCN-难络合,于是小组设计了如下实验:
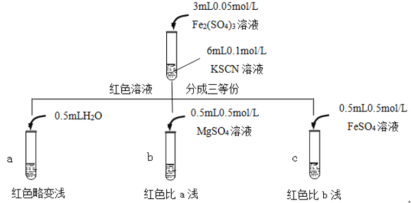
由此推测,实验II“红色明显变浅”的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4nH2O)是一种重要的食品和饲料添加剂。在实验室里可以通过下列流程用废铁屑制备。
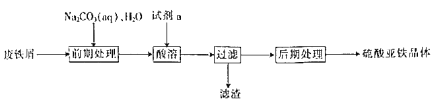
(1)试剂a是___(填写名称),上述流程中涉及的物质主要有①Na2CO3(aq)、②H2O、③试剂a、④废铁屑、⑤FeSO4nH2O,其中属于电解质的是___(填化学式),酸溶时发生的主要反应的化学方程式为___。
(2)上述流程中过滤操作所用的玻璃仪器有玻璃棒__、烧杯。
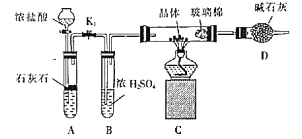
(3)利用如图装置对所得产品(FeSO4nH2O)结晶水的含量进行测定。反应前称量C中的硬质玻璃管(80g)、装入晶体后的硬质玻璃管(93g)。反应后称得C中硬质玻璃管的质量为87.6g。则产品硫酸亚铁晶体(FeSO4nH2O)中n=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)取3.0 g有机物X,完全燃烧后生成3.6 g水和3.36 L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为30,求该有机物的分子式________。X的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是_____(填标号)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(2)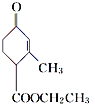 中的含氧官能团名称是________。
中的含氧官能团名称是________。
(3)分子式为C6H12 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为________,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为___________。
(4)肉桂酸苯甲酯G是一种香料,主要用于配制人造龙涎香,也可作皂用、化妆用及食用香精的调香原料。如图是用乙烯和甲苯为原料合成肉桂酸苯甲酯的路线图。
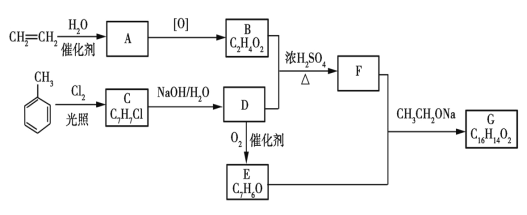
已知:RCHO+CH3COOR'![]() RCH=CHCOOR'。回答下列问题:
RCH=CHCOOR'。回答下列问题:
①A的结构简式是________,F的分子式是___________。
②C生成D的化学方程式是____________。
③D生成E的反应类型是__________。
④含有苯环,与D互为同分异构体的有机物有_____种(不考虑立体异构),其中不能与Na反应的结构简式是___________。
⑤G的结构简式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向纯水中加入NaOH使溶液的pH为11,则由NaOH电离出的OH 离子浓度和水电离出的OH离子浓度之比为 ( )
A.1:1B.108:1C.5×109:1D.1010:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com