
【题目】SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
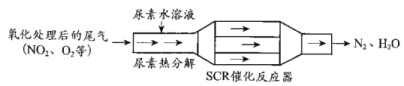
①尿素水溶液热分解为NH3和CO2,该反应的化学方程式:___。
②反应器中NH3还原NO2的化学方程式:___。
③当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:__。
④尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60g·mol-1)含量的方法如下:取ag尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1mLc1mol·L-1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L-1NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是__。
(2)NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。
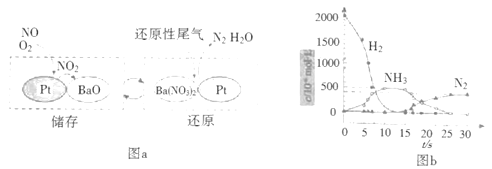
①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是__。
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是__。
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:___![]() □15NNO+□H2O___。
□15NNO+□H2O___。
【答案】CO(NH2)2+H2O![]() CO2+2NH3 8NH3+6NO2
CO2+2NH3 8NH3+6NO2![]() 7N2+12H2O 2SO2+O2+4NH3+2H2O=2(NH4)2SO4
7N2+12H2O 2SO2+O2+4NH3+2H2O=2(NH4)2SO4 ![]() BaO 8∶1 415NO+4NH3+3O2
BaO 8∶1 415NO+4NH3+3O2![]() 415NNO+6H2O
415NNO+6H2O
【解析】
结合反应物、生成物,根据原子守恒,若是氧化还原反应的方程式,再结合得失电子守恒配平化学反应方程式;测定溶液中尿素含量时,将所含氮完全转化为NH3,用过量的稀硫酸吸收氨气,反应后剩余的硫酸,用氢氧化钠溶液中和,整个过程中的,硫酸与氨气、氢氧化钠反应的化学方程式为2NH3+H2SO4=2(NH4)2SO4,2NaOH+H2SO4=2Na2SO4+2H2O。
(1)①尿素水溶液热分解为氨气和二氧化碳,反应方程式为CO(NH2)2+H2O![]() CO2+2NH3 ;
CO2+2NH3 ;
②NH3在催化剂作用下还原NO2生成N2和H2O,反应的化学方程式为8NH3+6NO2![]() 7N2+12H2O;
7N2+12H2O;
③二氧化硫在氧气作用下与氨气和水反应生成硫酸铵,此反应中二氧化硫是还原剂,氧气是氧化剂;反应的化学方程式为2SO2+O2+4NH3+2H2O=2(NH4)2SO4;
④NH3用过量的v1mLc1mol·L-1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L-1NaOH溶液恰好中和,过程中所涉及的化学方程式为:2NH3+H2SO4=2(NH4)2SO4,2NaOH+H2SO4=2Na2SO4+2H2O,反应中n(H2SO4)=c1×v1×10-3mol,n(NaOH)=c2×v2×10-3mol,由方程式可知:n(NaOH)+n(NH3)=2n(H2SO4),则n(NH3)=(2c1×v1×10-3-c2×v2×10-3)mol,n[CO(NH2)2]=![]() n(NH3)=
n(NH3)=![]() ×(2c1×v1×10-3-c2×v2×10-3)mol,m[CO(NH2)2]=60g·mol-1×
×(2c1×v1×10-3-c2×v2×10-3)mol,m[CO(NH2)2]=60g·mol-1×![]() ×(2c1×v1×10-3-c2×v2×10-3)mol=(0.06c1×v1-0.03c2×v2)g,所以尿素的质量分数是:
×(2c1×v1×10-3-c2×v2×10-3)mol=(0.06c1×v1-0.03c2×v2)g,所以尿素的质量分数是: ![]() =
=![]() ;
;
(2)①由图可知BaO和NOx反应生成Ba(NO3)2,Ba(NO3)2再被还原为
②第一步反应中H2被氧化生成水,氢元素化合价由0价升高到+1价,Ba(NO3)2中的N元素的化合价由+5价降到-3价,生成氨气,则1molBa(NO3)2生成氨气得到16mol电子,根据氧化还原反应中得失电子守恒,则参加反应的氢气的物质的量为![]() mol=8mol,故第一步反应消耗的H2与Ba(NO3)2的物质的量之比是8:1;
mol=8mol,故第一步反应消耗的H2与Ba(NO3)2的物质的量之比是8:1;
③在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO,由N元素守恒可知,15NO与NH3的物质的量之比应为1:1,结合氧化还原反应中得失电子守恒、原子守恒,可知该反应的化学方程式为:415NO+4NH3+3O2![]() 415NNO+6H2O。
415NNO+6H2O。


科目:高中化学 来源: 题型:
【题目】如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:

(1)请将分类依据代号填入相应的括号内:
(_____)两种物质都不是电解质
(_____)两种物质都是钠的化合物
(_____)两种物质都是氧化物
(_____)两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入上图中某种物质M的饱和溶液,继续煮沸至溶液呈红褐色.
①物质M的化学式为___。
②证明有红褐色胶体生成的实验操作是__。
(3)以下A~D四个涉及H2O2的反应,请填空:
A.Na2O2+2HCl=H2O2+2NaCl
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.![]() H2O2+
H2O2+![]() KMnO4+
KMnO4+![]() H2SO4→
H2SO4→![]() MnSO4+
MnSO4+![]() K2SO4+
K2SO4+![]() H2O+
H2O+![]() O2↑
O2↑
①配平D方程式,系数填在方框内__;该反应的还原剂是__;
②H2O2既体现氧化性,又体现还原性的反应是__,H2O2既不作氧化剂又不作还原剂的反应是__。(请用代号作答)
③请用双线桥法表示B反应中电子转移的方向和数目:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为
A. 2:1:1
B. 1:1:2
C. 1:2:1
D. 4:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫直接排放会危害环境。利用工业废碱渣(主要成分Na2CO3)可吸收烟气中的SO2并制备无水Na2SO3,其流程如图1。
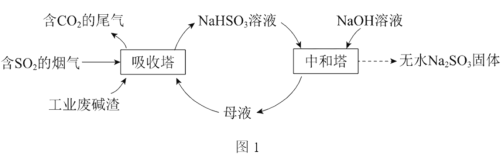
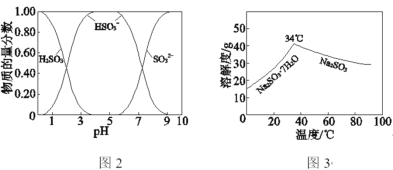
已知:H2SO3、HSO3、SO32在水溶液中的物质的量分数随pH的分布如图2,Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。
(1)Na2CO3溶液显碱性,用离子方程式解释其原因:_____________________。
(2)吸收烟气
①为提高NaHSO3的产率,应控制吸收塔中的pH为________。
②已知下列反应:
SO2(g)+2OH(aq)==SO32(aq)+H2O(l)ΔH1=164.3kJ·mol1
CO2(g)+2OH(aq)==CO32(aq)+H2O(l)ΔH2=109.4kJ·mol1
2HSO3(aq)==SO32(aq)+SO2(g)+H2O(l)ΔH3=+34.0kJ·mol1
吸收塔中Na2CO3溶液吸收SO2生成HSO3的热化学方程式是________。
③吸收塔中的温度不宜过高,可能的原因是________(写出1种即可)。
(3)制备无水Na2SO3
①中和塔中反应的离子方程式为_________________________________。
②从中和塔得到的Na2SO3溶液中要获得无水Na2SO3固体,需控制温度____________,同时还要_______________,以防止Na2SO3氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是 ( )
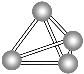
A. N4与N2互为同分异构体
B. N4分子中只含有共价键
C. 1 mol N4分子所含共价键数为4NA
D. N4沸点比P4(白磷)高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反-2-己烯醛(D)是一种重要的合成香料,下列合成路线是制备D的方法之一。根据该合成路线回答下列问题:
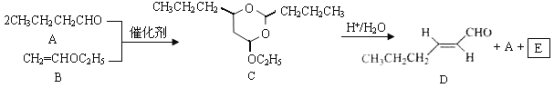
已知: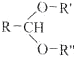
![]() RCHO+R'OH+R"OH
RCHO+R'OH+R"OH
(1)A的名称是__________;B分子中共面原子数目最多为__________;C分子中与环相连的三个基团中,不同化学环境的氢原子共有__________种。
(2)D中含氧官能团的名称是__________,写出检验该官能团的化学反应方程式:__________。
(3)E为有机物,能发生的反应有__________。
a.聚合反应b.加成反应c.消去反应d.取代反应
(4)B的同分异构体F与B有完全相同的官能团,写出F所有可能的结构:________。
(5)以D为主要原料制备己醛(目标化合物),在方框中将合成路线的后半部分补充完整。
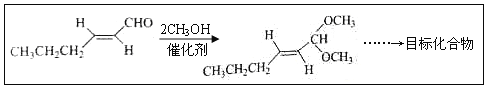
(6)问题(5)的合成路线中第一步反应的目的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L1NaOH溶液500 mL。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,还需要的玻璃仪器是________。
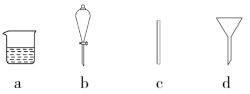
(2)根据计算用托盘天平称取的NaOH固体质量为__________g。
(3)关于容量瓶的四种叙述:
①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是______(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)容量瓶上需标有以下五项中的_________________(填序号)。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(5)配制时,其正确的操作顺序是_________(用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(6)下列配制的溶液浓度偏低的是____________(填序号)。
A.称量NaOH时,砝码错放在左盘
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
E.配制前,容量瓶中有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.5g NaOH、NaHCO3、Na2CO3固体粉末溶于水,制成溶液,然后逐渐向其中滴加1mol/L的盐酸,所加入盐酸的体积与产生的CO2的体积(标准状况)的关系如图像所示:
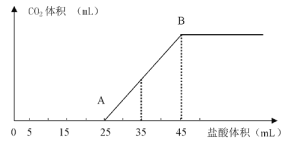
(1)写出OA段发生的离子反应方程式___________________、___________________________
(2)当加入35mL盐酸时,产生CO2的体积为_________________(标准状况)
(3)原混合物中NaOH的质量为_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com