
镁、铝、铁是重要的金属,在工业生产中用途广泛。
(1)镁与稀硫酸反应的离子方程式为 ;
(2)铝与氧化铁发生铝热反应的化学方程式为 ;
(3)在潮湿的空气里,钢铁表面有一层水膜,很容易发生电化学腐蚀。其中正极的电极反应式为 ;
(4)铝在空气中具有很好的抗腐蚀性能,铝制品在日常生活中被广泛应用。在海洋工程上,通常用铝合金(Al—Zn—Cd)保护海底钢铁设施,其原理如图18所示: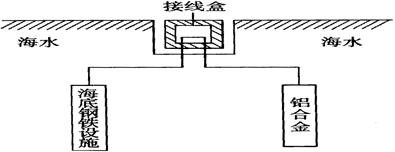
其中负极发生的电极反应为 ;
在实际应用中,用铝合金而不选用纯铝。纯铝不能很好地起到保护作用,其原因是 。
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:填空题
100ml 2mol/LNaOH溶液中通入一定量的CO2,反应后溶液中Na2CO3和NaHCO3的物质的量浓度之比为1∶2。则:
(1)写出其中生成Na2CO3的反应的离子方程式: 。
(2)生成碳酸氢钠的物质的量为 mol。
(3)若往原NaOH溶液中通入标准状况下的CO2气体1.12L后,再逐滴滴加0.5mol/L的盐酸,至少加入 ml后才会有CO2气体放出(不考虑CO2溶解在水中)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铁和铝是生产和生活中最常见的两种金属,其单质和化合物被广泛应用。
(1)硫酸铁溶液可用于浸出黄铜矿精矿,其主要反应为:
CuFeS2+4Fe3+=Cu2++5Fe2++2S(CuFeS2中S为-2价,Fe为+2价)。
关于该反应,下列说法中,正确的是 (选填序号);
a.从物质分类的角度看,CuFeS2属于合金 b.反应过程中只有一种元素被还原
c.CuFeS2既作氧化剂又作还原剂 d.当转移1 mol电子时,产生16 g S
(2)高铁酸钾(K2FeO4)是一种新型水处理剂,在水中发生反应生成Fe(OH)3胶体。该反应中,高铁酸钾表现 (填“氧化性”或“还原性”),Fe(OH)3胶体具有净水作用,其原因是 。
(3)某同学取一张铝箔,并用针刺一些小孔,然后取一药匙过氧化钠粉末,用铝箔包好,放入右图所示装置内倒扣的漏斗中(图中铁架台和铁夹没有画出)。
按顺序写出该过程中发生反应的离子方程式:
① ;
② 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
已知NaHCO3在低温下溶解度较小。
反应Ⅰ:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl,处理母液的两种方法:
NaHCO3↓+NH4Cl,处理母液的两种方法:
(1)向母液中加入石灰乳,可将其中________循环利用。
(2)向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式 ___________。
Ⅱ.某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装置制取NaHCO3,然后再将NaHCO3制成Na2CO3。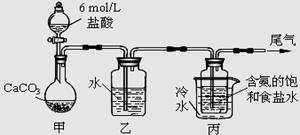
(1)装置丙中冷水的作用是 ;
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有_______、洗涤、灼烧。NaHCO3转化为Na2CO3的化学方程式为 ;
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如图所示。
则曲线a对应的溶液中的离子是___________(填离子符号下同);曲线c对应的溶液中的离子是___________;该样品中NaHCO3和Na2CO3的物质的量之比是 ; 21
(4)若取21.0 g NaHCO3固体,加热了t2 rnin后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol?L—1的盐酸中,则充分反应后溶液中H+ 的物质的量浓度为____________(设溶液体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下列物质之间有如下反应关系: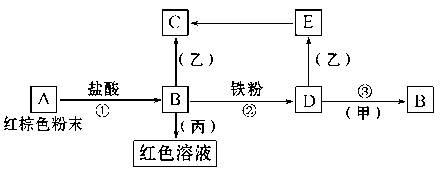
已知由E转化成C的现象是:白色沉淀迅速变为灰绿色,最后变为红褐色。回答:
(1)写出下列物质的化学式:甲________,丙________。
(2)写出E→C反应的化学方程式:___________________________。为了获得E,可以用新配制的D溶液与用不含O2的蒸馏水配制的乙溶液反应制备。
(3)用相应晶体配制上述D溶液时你觉得还需加入 。
(4)写出Fe与H20在一定条件下反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
将10.1克过氧化钠和钠的混合物跟120.1克水充分反应后,收集到的气体体积在标准状况下为2.24L。
(1)试分别写出过氧化钠跟水反应的离子、化学方程式 ;(2)计算原混合物中过氧化钠和氧化钠的物质的量之比,n(Na2O2):n(Na)= 。
(3)计算所得溶液的质量分数是多大?ω= 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)利用化学反应可以制备许多物质。实验室用铜制备NO2的离子方程式为_____________ ______。
(2)工业上,黄铜矿(主要成分CuFeS2)是提取铜的主要原料,可采用火法溶炼工艺生产铜,该工艺的中间过程会发生反应:Cu2S+2Cu2O===6Cu+SO2↑。该反应中还原剂为_______ (填化学式),每生成1mol Cu,反应中转移电子的物质的量为___________。
黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。 ②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。 据以上信息回答下列问题:
a.通过上述②,炉渣中的Al2O3变成了 (写离子)。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 酸性KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
根据下列转化关系以及现象回答: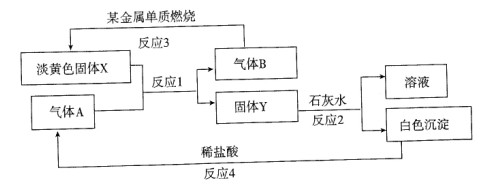
(1)固体X的名称是 ,Y的化学式是 。
(2)写出反应l的化学方程式 。
(3)写出反应2的化学方程式 。
(4)若15.6g X和足量水反应,转移 mol e-。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上通常以铝土矿(主要成分为Al2O3)为原料制备无水氯化铝:2Al2O3+6Cl2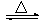 4AlCl3+3O2 ↑。请回答下列问题:
4AlCl3+3O2 ↑。请回答下列问题:
(1)上述反应涉及的元素中,最外层有2个未成对电子的元素是__________;简单离子的离子半径最小的元素,其原子核外有_____种不同能级的电子。
(2)已知元素周期表中,镓(31Ga)与铝元素同一主族,写出Ga的最外层电子排布式:______
(3)镓(Ga)有两种天然同位素,一种是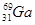 ,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
(4)为促进反应的进行,实际生产中需加入焦炭,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com