
【题目】感光性高分子也称“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料,其结构简式如下

试回答下列问题:
(1)在一定条件下,该高聚物可发生的反应有(填写编号)________。
①加成反应 ②氧化反应 ③消去反应 ④酯化反应 ⑤卤代反应
(2)该高聚物在催化剂的作用下水解得到相对分子质量较小的产物A,A的同分异构体有多种,其中含有苯环、 ,且苯环上有两个处于对位的取代基的物质的结构简式可能是__________________。
,且苯环上有两个处于对位的取代基的物质的结构简式可能是__________________。
科目:高中化学 来源: 题型:
【题目】实验室需要400mL 0.5molL﹣1的稀硫酸溶液,现用密度为1.84gmL﹣1 , 质量分数为98%浓硫酸来配制,请回答下列问题:
(1)若要实施配制,下列仪器中,不会用到的是(填字母).
A.250mL容量瓶;
B.500mL容量瓶;
C.托盘天平;
D.量筒;
E.烧杯;
F.玻璃棒
(2)配制过程中,除上述仪器外,尚缺的仪器是 .
(3)未冷却至室温立即转移硫酸溶液,则所配硫酸溶液的浓度(填“偏高”、“偏低”或“无影响”,下同);若定容时,滴加蒸馏水不慎超过了刻度线,则所配硫酸溶液的浓度 .
(4)通过计算,用量筒量取mL浓硫酸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. Fe3O4溶于足量稀硝酸:Fe3O4+8H+=Fe2++2Fe3++4H2O
B. 漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
C. MnO2与浓盐酸反应制Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D. 在强碱溶液中,次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮和磷为周期表中的第VA族元素,它们的元素及其化合物在性质上既有相似性又有不同性。回答下列问题:
(1)N2分子中两个N原子都达到8电子稳定状态,则两个N原子之间共有电子的数目为____________;白磷的分子式为P4,4个P原子相互之间共形成6个共价单键,且每个P原子都达到8电子稳定状态,则白磷分子的空间构型为____________。
(2)N、P两种元素都能形成多种气态氢化物。联氨(N2H4)为二元弱碱,在水中的电离与氨相似,写出联氨在水中第一步电离方程式___________________________,联氨与磷酸(H3PO4)形成的磷酸二氢盐的化学方程式为_________________________________。
(3)P2O5是一种干燥剂,下列气体不能用P2O5干燥的是________(填字母序号)。
A.SO2 B.NH3 C.CO D.H2 E.H2S F.O2
(4)次磷酸(H3PO2)是一元中强酸,它的工业制法是将白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式________,Ba(H2PO2)2为_______________(填“正盐”或“酸式盐”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明碳酸比硅酸酸性强的实验事实是( )
A. CO2是气体,SiO2是固体 B. 高温下,二氧化硅和碳酸钠能反应
C. CO2溶于水生成碳酸,而SiO2却不溶于水 D. CO2通入NaSiO3溶液中有胶状沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水常用Cl2消毒,某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是( )
A. AgNO3 B. FeCl2 C. Na2SO3 D. AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用下图装置可进行测定SO2转化成SO3转化率的实验探究:
已知:SO3的熔点是16.8℃,沸点是44.8℃。

(1)请从下图A~F装置中选择最适合装置并将其序号填入下面的空格中Ⅰ____________、Ⅱ___________、Ⅲ___________。

![]()
![]()



冰水 浓硫酸 生石灰 水 NaOH溶液 热水
A B C D E F
(2)用1mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了12.8g,则实验中SO2的转化率为_______ % 。
(3)为使SO2有较高的转化率,应均匀通入O2,,且试验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作顺序是________________;尾端球形干燥管的作用是_____________。
(4)将S02通过Na2O2粉末,完全反应后除生成O2外还生成一种白色粉末。证明该白色粉末既有Na2SO3又有Na2SO4所需的试剂是水、_______、________、品红溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置进行相应的实验,不能达到实验目的的是( )
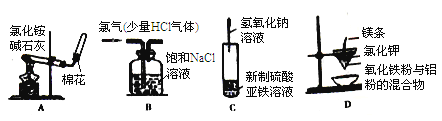
A.实验室制取并收集氨气 B.除去Cl2中的HCl气体杂质
C.实验室制取氢氧化亚铁 D.铝热反应实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe与稀HNO3反应时,若两者消耗物质的量之比为4∶10,且生成 Fe(NO3)2,则反应中生成的还原产物可能是( )
A.N2B.N2OC.NOD.NH4NO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com