
【题目】柠檬醛的结构简式如图所示,主要用作柠檬和什锦水果型香精,也是合成紫罗兰酮的主要原料

(1)柠檬醛不能发生的反应类型为_____________(填字母)。
A.酯化反应 B.加成反应 C.氧化反应 D.消去反应
(2)香叶醇经催化氧化可制得柠檬醛,则香叶醇的结构简式为_____________
(3)双羟基香茅酸(![]() 也是一种重要的香料,可由柠檬醛合成,合成路线如下
也是一种重要的香料,可由柠檬醛合成,合成路线如下

双羟基香茅酸的分子式为________,写出A→B的化学方程式___________________________
科目:高中化学 来源: 题型:
【题目】某科研小组利用工业废料(主要成分NiO,含有少量Al2O3、FeO、CuO、BaO)回收NiO,并制备其他部分产品的工艺流程如下:

已知:①溶液中离子浓度小于等于1.0×10-5 mol·L-1时,认为该离子沉淀完全。
②25℃时,部分难溶物的溶度积常数如下表所示:
难溶物 | CuS | Al(OH)3 | Ni(OH)2 | Fe(OH)3 | Fe(OH)2 |
溶度积常数(Ksp) | 6.3×10-36 | 1.3×10-33 | 2.0×10-15 | 4.0×10-38 | 1.8×10-16 |
请回答下列问题:
(1)H2S的电子式为_______________________________。
(2)“酸浸”时,Ni的浸出率与温度的关系如图所示。 温度高于70℃,Ni的浸出率降低的主要原因为___________________________________________________________。

(3)“沉淀1”的主要成分为____________________(填化学式)。
(4)“滤液1”中通入H2S的作用为___________________。
(5)“转化”过程中,发生反应的主要离子方程式为________________________________。
(6)25℃时,“调节pH2”使沉淀3中金属阳离子沉淀完全后,所得溶液中的C(H+)最大为____________(保留三位有效数字,已知![]() ≈1.4)。
≈1.4)。
(7)“操作I”主要包括蒸发浓缩、__________________、过滤、洗涤、干燥。
(8)NiO可通过铝热反应冶炼Ni,该反应的化学方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
以芳香化合物A和有机物D为原料,制备异戊酸薄荷醇酯(M)和高聚物(N)的一种合成路线如下:

已知:I.A→B的原子利用率为100%。
Ⅱ. (R1、R2表示氢原子或烃基)
(R1、R2表示氢原子或烃基)
请回答下列问题:
(1)A的结构简式为___________。
(2)D的化学名称为___________。
(3)G的核磁共振氢谱中有___________组吸收峰。
(4)F→H的反应类型为_______________________。
(5)C+G→M的化学方程式为_____________________________________________。
(6)同时满足下列条件的B的同分异构体有___________种(不考虑立体异构)。
①苯环上连有两个取代基
②能发生银镜反应
(7)参照上述合成路线和信息,以乙烯为原料(无机试剂任选),设计制备 的合成路线:_____________________________________________________________________。
的合成路线:_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经测定由C3H7OH和C6H12组成的混合物中氧的质量分数为8%,则此混合物中氢的质量分数是
A. 78% B. 22% C. 14% D. 13%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数。
③向锥形瓶中滴入甲基橙作指示剂,进行滴定。到达滴定终点时测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)滴定终点的判断方法是______________________________________________。
(2)有错误操作步骤有_______________。
(3)如图,是某次滴定时的滴定管中的液面,其读数为___________mL

(4)则待测烧碱溶液的浓度为___________mol/L。
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前度数(mL) | 滴定后度数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强氧化剂[RO〔OH〕2]2+离子中的元素R可被亚硫酸钠还原到较低价态。假设把1.2×10-3mol[RO(OH)2]2+还原,需要消耗6mL0.2mol/L的亚硫酸钠溶液,那么反应后R的化合价为
A.0B.+2C.+3D.+4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(gmol﹣1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.075 | 170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是(填写物质的序号).
A.蔗糖
B.硫酸钾
C.高锰酸钾
D.硝酸银
(2)为配制500mL上述“鲜花保鲜剂”所需的玻璃仪器有:烧杯、玻璃棒、量筒、、 . (在横线上填写相应仪器的名称),
(3)某同学取用保鲜剂固体配制溶液的过程如图所示,其错误操作序号是 
(4)在溶液配制过程中,下列实验操作会使配得的溶液浓度偏大的是 .
A.溶解固体时,未冷却就直接转移
B.转移溶液后未洗涤烧杯和玻璃棒就直接定容
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G( )是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
)是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
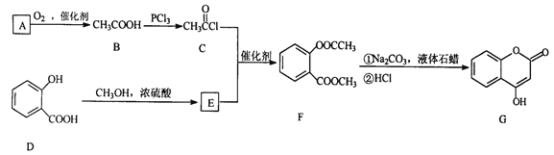
(1)A与银氨溶液反应有银镜生成,则A的结构简式是__________________;D中官能团名称为_______; B→C的反应类型是_____________反应。
(2)下列关于G的说法不正确的是_______________(填字母)
A.1molG最多能和5mol氢气反应 B.能与金属钠反应
C.能与溴的四氯化碳溶液反应 D.分子式是C9H6O3
(3)写出一种满足下列条件的E的同分异构体的结构简式:_________________________。
①苯环上的一氯取代产物只有两种;②能发生银镜反应;③能与FeCl3溶液发生显色反应
(4)写出F和过量NaOH溶液共热时反应的化学方程式:_______________________________。
(5)请设计合理的方案以苯酚和乙醇为原料合成乙酸苯酯(![]() )(用合成路线流程图表示,并注明反应条件)。提示:①合成过程中无机试剂任选;②合成反应流程图表示方法示例如下:
)(用合成路线流程图表示,并注明反应条件)。提示:①合成过程中无机试剂任选;②合成反应流程图表示方法示例如下:![]() ____________________。
____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.标准状况下,22.4 L H2O中含有氢原子数目为2NA
B.17 g NH3所含质子数为10NA
C.0.1mol Cu(NO3)2中含有的离子数目为0.2NA
D.28g N2 体积为22.4L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com