
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
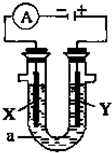 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 装置编号 | A | B | C | D | E |
| 试 剂 | 硝酸银溶液 | 澄清石灰水 | 氧化铜粉末 | 澄清石灰水 | 无水硫酸铜 |
| 现 象 | 无明显变化 | 变浑浊 | 变红色 | 无明显变化 | 变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量铁粉,然后过滤 |
| B、Na2O2用于呼吸面具,活性炭用于防毒面具,两者原理不同 |
| C、NaOH、Na2CO3、NaHCO3的溶液均呈碱性,所以可以共存 |
| D、62g Na2O和78g Na2O2分别溶于等量且足量的水中,所得溶液中溶质的质量分数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 垃圾 | 非易拉罐 | 废塑料瓶 | 废荧光灯管 | 不可再生塑料 |
 可回收物 |  其它垃圾 |  有害垃圾 |  可燃垃圾 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com