
 根据下列图示变化及已知条件填空.
根据下列图示变化及已知条件填空.分析 A为一气态有机物,标准状况时2.24LA恰好含有16g溴的溴水褪色,说明A分子中含有一个碳碳双键,A与水加成得B为醇,B经过两步氧得D为羧酸,G在浓硫酸作用下生成H,H和A为同系物,并比A多一个碳原子,则G为醇,完全燃烧10mLE的蒸气需65mL氧气,同时产生50mLCO2和50mL水蒸汽,根据元素守恒可知,E的分子式为C5H10O2,所以可以推知E为CH3COOCH2CH2CH3,根据转化关系可知,A为CH2=CH2,B为CH3CH2OH,B氧化得C为CH3CHO,C氧化得D为CH3COOH,D与G发生酯化反应得E,则G为HOCH2CH2CH3,E发生碱性水解得F为CH3COONa,G在浓硫酸加热的条件下生成H为CH3CH=CH2,据此答题.
解答 解:A为一气态有机物,标准状况时2.24LA恰好含有16g溴的溴水褪色,说明A分子中含有一个碳碳双键,A与水加成得B为醇,B经过两步氧得D为羧酸,G在浓硫酸作用下生成H,H和A为同系物,并比A多一个碳原子,则G为醇,完全燃烧10mLE的蒸气需65mL氧气,同时产生50mLCO2和50mL水蒸汽,根据元素守恒可知,E的分子式为C5H10O2,所以可以推知E为CH3COOCH2CH2CH3,根据转化关系可知,A为CH2=CH2,B为CH3CH2OH,B氧化得C为CH3CHO,C氧化得D为CH3COOH,D与G发生酯化反应得E,则G为HOCH2CH2CH3,E发生碱性水解得F为CH3COONa,G在浓硫酸加热的条件下生成H为CH3CH=CH2,所以A的名称为乙烯,B的名称为乙醇,C的名称为乙醛,D的名称为乙酸,E的名称为乙酸丙酯,F的名称为乙酸钠,G的名称为1-丙醇,H的名称为丙烯,各步反应的方程式及反应类型依次为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,加成反应;2CH3CH2OH+O2$\stackrel{催化剂}{→}$2CH3CHO+H2O,氧化反应;2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH,氧化反应;HOCH2CH2CH3+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH3+H2O,酯化反应;CH3COOCH2CH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2CH2OH,水解反应;CH3CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$CH3CH=CH2+H2O,消去反应,
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,加成反应;2CH3CH2OH+O2$\stackrel{催化剂}{→}$2CH3CHO+H2O,氧化反应;2CH3CHO+O2$\stackrel{催化剂}{→}$2CH3COOH,氧化反应;HOCH2CH2CH3+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH3+H2O,酯化反应;CH3COOCH2CH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2CH2OH,水解反应;CH3CH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$CH3CH=CH2+H2O,消去反应.
点评 本题侧重于有机物的推断的考查,同时考查学生对知识的整合能力和计算能力,难度中等,注意根据元素守恒和有机反应物之间量的关系进行推断.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 12种 | B. | 4种 | C. | 8种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电负性的大小可以作为判断金属性和非金属性强弱的尺度 | |
| B. | 在同一电子层上运动的电子,其自旋方向肯定不同 | |
| C. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| D. | 原子最外层电子排布是5s1的元素,其氢氧化物一定不能溶解氢氧化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | |
| B. | 利用腐蚀法制作印刷线路板:2Fe3++Cu═2Fe+Cu2+ | |
| C. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 实验室用液溴和苯在催化剂作用下制溴苯: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
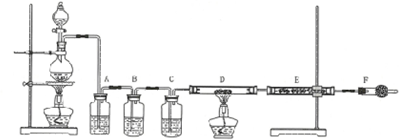 过量的锌与浓硫酸作用的全过程中产生的气体可能有多种.有人认为气体中可能有SO2,也可能有H2.为了说明这两种气体的有无,设计了如图所示的实验装置.
过量的锌与浓硫酸作用的全过程中产生的气体可能有多种.有人认为气体中可能有SO2,也可能有H2.为了说明这两种气体的有无,设计了如图所示的实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 引起日本水俣病的重金属是镉 | |
| B. | 引起日本痛痛病的重金属是汞 | |
| C. | 水体富营养化是因为大量含Na+的肥皂水任意排放造成的 | |
| D. | 改善水质最主要的是控制工业废水和生活污水的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将58.5 g NaCl溶于1 L水中,可得1 mol/L的NaCl溶液 | |
| B. | 可使用250 mL容量瓶分两次完成490 mL某浓度的BaCl2溶液的配制 | |
| C. | 将25.0 g胆矾溶于水后配成100 mL溶液所得溶液浓度为1 mol/L | |
| D. | 将78 g Na2O2溶于水配成1 L溶液,可得到浓度为1 mol/L的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com