
【题目】一定条件下,恒容的密闭容器中存在反应:2A(g)+B(s) ![]() 2C(g) △H<0。下列描述中能证明上述反应已达平衡状态的是
2C(g) △H<0。下列描述中能证明上述反应已达平衡状态的是
A.摩尔质量:A<C
B.容器中混合气体的密度不随时间而变化
C容器中的气体压强不随时间而变化
D.容器中A与C的物质的量之比等于1:1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】按题目要求答题:
(1)CH3CH2C(CH3)2CH(C2H5)CH3的系统命名是___________________;
(2)写出甲苯与浓硫酸、浓硝酸的混合酸在100℃发生取代反应的化学方程式:_______________;
(3)写出下列各有机物的结构简式
①支链只有一个乙基且式量最小的烷烃____________________;
②某烃类化合物A的相对分子质量为84,能与氢气发生加成反应。A的一氯取代产物只有一种,则A的结构简式为 ;
③二甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效,具有优良的环保性能。写出与二甲醚相对分子质量相等且元素种类相同的所有有机物的结构简式是:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是( )
4NO(g)+6H2O(g),下列叙述中正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达平衡状态
C. 达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
D. 平衡混合物中各物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选用的除杂试剂和实验操作都正确的(已知2Br﹣+Cl2═Br2+2Cl﹣)是( )
选项 | 物质 | 杂质 | 除杂试剂 | 操作方法 |
A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙 | 过滤 |
B | NaCl溶液 | NaBr | 稍过量氯水、乙醇 | 萃取、分液 |
C | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液 | 过滤 |
D | O2 | CO | 氧化铜 | 通过灼热的氧化铜 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO: MgSO4(s)+CO(g) ![]() MgO(s)+CO2(g)+SO2(g) △H >0,该反应在某密闭容器中达到平衡。下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H >0,该反应在某密闭容器中达到平衡。下列分析正确的是
A. 恒温恒容时,充入CO气体,达到新平衡时![]() 增大
增大
B. 容积不变时,升高温度,混合气体的平均相对分子质量减小
C. 恒温恒容时,分离出部分SO2气体可提高MgSO4的转化率
D. 恒温时,增大压强平衡逆向移动,平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y ![]() 2Z,其平衡常数为1600(mol/L) -2
2Z,其平衡常数为1600(mol/L) -2
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,下列说法中正确的是
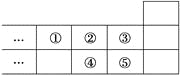
A. 元素①位于第2周期第ⅣA族
B. 气态氢化物的稳定性:④>②
C. 最高价氧化物对应水化物的酸性:⑤>④
D. 元素的最高正化合价:③=⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
Ⅰ.已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=a kJ·mol-1
②CO(g)+l/2O2(g)=CO2(g) ΔH=b kJ·mol-1
③C(石墨)+O2(g)=CO2(g) ΔH=c kJ·mol-1
则反应4Fe(s)+3O2(g)=2Fe2O3(s)的焓变ΔH=______________kJ·mol-1。
Ⅱ.依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是_____(填序号)。
C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的正极反应式为______________________。
Ⅲ.金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如下图所示。

①在通常状况下,金刚石和石墨中________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为________。
②12 g石墨在一定量空气中燃烧,生成气体36 g,该过程放出的热量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡 向________(填“正”或“逆”)反应方向移动;溶液中![]() 的值________(填“增大”、“减小”或“不变”)。
的值________(填“增大”、“减小”或“不变”)。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5 mol·L-1;
b.CH3COOH+NaHCO3===CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________性,NH4HCO3溶液中物质的量浓度最大的离子是________(填化学式)。
(3)99 ℃时,KW=1.0×10-12 mol2·L-2,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为________________。
②该温度下,将0.01 mol·L-1H2A溶液稀释到20倍后,溶液的pH=__________。
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气____________。
A.盐酸多 B.H2A多 C.一样多 D.无法确定
④将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com